Les régions périanale, périnéale et périgénitale du chien constituent un territoire anatomique d’une complexité souvent sous-estimée en consultation courante. Pourtant, les dermatoses qui y siègent sont fréquentes, polymorphes et susceptibles d’engendrer une morbidité significative. Prurit rebelle, douleur chronique, lésions ulcératives ou nodulaires : autant de tableaux cliniques qui exigent une démarche diagnostique structurée. A l’occasion du dernier congrès ESVD, notre consœur Elisa Maina de l’université de Bern, a fait un point complet sur ces différentes dermatoses.
La multiplicité des structures anatomiques concentrées dans cette zone, sacs anaux, glandes hépatoïdes, épithélium squameux kératinisé, organes génitaux externes, explique la diversité nosologique des affections rencontrées. Du simple prurit allergique à la néoplasie à potentiel métastatique élevé, en passant par la fistule périanale immuno-médiée, chaque entité clinique requiert une reconnaissance précise et une prise en charge thérapeutique adaptée. La région périnéale, quant à elle, se distingue par son exposition permanente aux matières fécales, à l’urine et aux agents irritants exogènes, ce qui en fait une zone de vulnérabilité dermatologique particulière. La région périgénitale, qui comprend les organes génitaux externes des deux sexes, présente ses propres spécificités cliniques, depuis l’intertrigo vulvaire chez la femelle jusqu’à la dermatite scrotale chez le mâle.
Bases Anatomiques : Un Prérequis Clinique Incontournable
Architecture de la Région Périanale
La région périanale est structurellement plus complexe que sa seule apparence externe ne le laisse supposer. L’anus se subdivise en trois zones fonctionnellement et histologiquement distinctes. La zone colonnaire, la plus proximale, est directement rattachée à la muqueuse rectale. La zone intermédiaire représente une zone de transition. Enfin, la zone cutanée, constituée d’un épithélium squameux kératinisé, revêt une importance clinique de premier ordre : c’est elle qui abrite les glandes hépatoïdes, également désignées glandes circumanales ou glandes périanales ainsi que les orifices des canaux excréteurs des sacs anaux.
Cette distinction anatomique n’est pas anodine. Nombre d’affections présentent un tropisme électif pour l’une ou l’autre de ces sous-zones, ce qui conditionne directement leur expression clinique et leur diagnostic différentiel. Confondre une atteinte de la zone cutanée avec une pathologie strictement muqueuse ou rectale constitue une erreur diagnostique aux conséquences thérapeutiques potentiellement délétères. La zone cutanée périanale, de par la nature de son épithélium kératinisé et la densité des structures glandulaires qu’elle concentre, représente le siège de prédilection des néoplasies des glandes hépatoïdes et des processus inflammatoires chroniques tels que la fistule périanale. Sa reconnaissance clinique précise est donc un prérequis incontournable à toute démarche diagnostique sérieuse dans cette région.
Les Sacs Anaux : Structure, Contenu et Physiologie
Les sacs anaux, encore appelés sacs périanaux, sont deux poches bilatérales nichées dans le tissu sous-cutané, dont les canaux excréteurs débouchent précisément dans la portion cutanée de l’anus. Leur paroi est composée de deux types glandulaires : des glandes sébacées, distribuées principalement le long du canal, et des glandes apocrines, tapissant la paroi interne du sac proprement dit. Le contenu de ces structures résulte de la combinaison de ces sécrétions glandulaires, auxquelles s’ajoutent des kératinocytes desquamés et du liquide. Ce mélange présente des caractéristiques individuelles notables en termes de couleur, de consistance et d’odeur, ce qui explique la variabilité macroscopique observée d’un animal à l’autre lors de l’examen clinique.
La vidange physiologique de ce contenu s’effectue par un mécanisme mécanique : la pression exercée par le bol fécal lors du transit, couplée à la contraction de la musculature périnéale au moment de la défécation. Ce mécanisme physiologique est donc étroitement dépendant de la consistance des selles, du tonus musculaire périnéal et de l’absence d’obstruction canalaire. Lorsque ces mécanismes sont insuffisants, en raison d’une consistance anormale des fèces, d’un défaut tonique musculaire ou d’une inflammation locale, le contenu s’accumule et peut évoluer vers des états pathologiques progressivement plus graves, depuis l’impaction jusqu’à l’abcès en passant par la sacculite. La compréhension de cette physiologie est indispensable pour identifier les facteurs prédisposants et prévenir les récidives.
La Région Périnéale et Périgénitale
La région périnéale correspond anatomiquement à la zone losangique délimitée crânialement par la base de la queue et caudalement par la base des organes génitaux externes. Son exposition permanente à l’urine, aux matières fécales et aux agents irritants exogènes en fait une zone particulièrement vulnérable aux dermatoses, d’autant plus dans les races présentant une densité pilleuse réduite en regard de cette zone. Cette faible protection pileuse laisse l’épiderme directement exposé aux agents chimiques et mécaniques issus de l’environnement immédiat, facilitant ainsi le développement de dermatites irritatives, de surinfections bactériennes ou fongiques et de lésions de macération chronique. La région périgénitale, quant à elle, englobe les organes génitaux externes des deux sexes, avec des entités cliniques spécifiques selon le genre, intertrigo vulvaire chez la femelle, dermatite scrotale chez le mâle, qui seront abordées dans les sections dédiées. Les tumeurs périgénitales, bien que moins fréquentes que celles de la région périanale, constituent également un diagnostic différentiel à considérer devant toute masse à croissance progressive dans cette localisation.
Sémiologie et Approche Diagnostique Initiale
Interpréter les Comportements : Traîneau et Léchage
Le praticien confronté à un chien présenté pour léchage ou frottement de la région périanale sur le sol doit d’emblée replacer ces comportements dans leur contexte physiologique avant d’en conclure à une pathologie. Des données publiées indiquent que 24 % des chiens cliniquement sains adoptent spontanément ce comportement de « traîneau », tandis que 36 % se lèchent la région périanale avec une intensité moyenne évaluée à 3,5 sur une échelle de 10. Ces chiffres témoignent de la variabilité comportementale normale et invitent à la prudence dans l’interprétation. Le léchage et le frottement de la région périanale peuvent en effet s’inscrire dans des comportements de toilettage parfaitement physiologiques chez l’espèce canine.
C’est l’augmentation de la fréquence et de l’intensité de ces comportements, par rapport au comportement de base de l’animal, qui doit alerter le clinicien et orienter vers une pathologie subclinique ou clinique. Un léchage excessif, une irritabilité accrue lors de la manipulation de la région, ou une automutilation doivent être considérés comme des signaux d’alarme justifiant un examen approfondi. L’anamnèse doit systématiquement préciser l’ancienneté des signes, leur caractère permanent ou intermittent, l’existence d’épisodes digestifs récents, notamment des épisodes diarrhéiques, et les antécédents allergiques ou dermatologiques connus de l’animal. Ces informations permettent d’orienter précocement la démarche diagnostique vers l’une des grandes catégories étiologiques : affections des sacs anaux, dermatoses allergiques, processus immuno-médiés ou néoplasies.
Différencier Affection des Sacs Anaux et Dermatose Cutanée Stricte
La première étape diagnostique, face à ces signes d’appel, consiste à établir si l’origine est glandulaire, c’est-à-dire liée aux sacs anaux, ou purement cutanée. Cette distinction conditionne l’ensemble de la démarche ultérieure. L’examen rectal par palpation interne digitale demeure la méthode de référence : elle permet d’évaluer la symétrie des sacs, leur degré de réplétion, la présence d’une douleur provoquée et la consistance du contenu. Un examen superficiel se limitant à l’observation externe sans palpation interne est insuffisant et expose à des erreurs diagnostiques par défaut de caractérisation lésionnelle. La douleuyr parfosi présenet est néanmoins à prendre en compte avant sa réalisation.
Un point mérite d’être souligné, car il est source d’erreurs diagnostiques fréquentes : l’évaluation macroscopique et microscopique du contenu des sacs anaux n’est pas prédictive de la maladie. Des bactéries, aussi bien intracellulaires qu’extracellulaires, des neutrophiles et des levures de type Malassezia se retrouvent régulièrement dans les prélèvements issus de sacs anaux de chiens sains. La culture bactériologique systématique du contenu, réalisée sans contexte clinique d’abcès avéré, n’apporte donc pas de valeur diagnostique isolée. Le praticien qui fonderait sa décision thérapeutique sur ces seuls résultats cytologiques ou microbiologiques s’exposerait à des erreurs de prescription, notamment une antibiothérapie injustifiée. Le diagnostic repose fondamentalement sur la mise en évidence d’une inflammation tissulaire cliniquement détectable et d’une douleur provoquée à la palpation.
Affections des Sacs Anaux : Du Fonctionnel au Pathologique
Les affections non-néoplasiques des sacs anaux représentent une cause fréquente de consultation en médecine générale vétérinaire, avec une prévalence annuelle estimée à 4,40 % dans les cabinets britanniques de première intention. L’impaction en constitue la forme la plus courante, représentant près de 79 % des cas, suivie par la sacculite (12 %) et l’abcès (9 %). Des prédispositions raciales marquées ont été documentées : les types brachycéphales présentent 2,6 fois plus de risque de développer une affection des sacs anaux que les types dolichocéphales. Le Cavalier King Charles Spaniel, le King Charles Spaniel, les Cockapoos et les Bichons Frisés comptent parmi les races les plus exposées. À l’inverse, le Labrador Retriever, le Berger Allemand, le Border Collie et le Boxer présentent un risque réduit par rapport aux chiens croisés. Ces données épidémiologiques ont des implications pratiques directes : la race doit être intégrée dans la stratification du risque lors de l’anamnèse, et l’identification systématique d’une maladie allergique sous-jacente, notamment la dermatite atopique, première comorbidité associée aux sacculites récidivantes, conditionne l’efficacité de la prise en charge à long terme.
Un Continuum Évolutif : Impaction, Sacculite et Abcès
Ces trois entités cliniques ne constituent pas des entités indépendantes mais les stades successifs d’un même processus pathologique évolutif. La compréhension de ce continuum est indispensable pour adapter la prise en charge à chaque étape et pour anticiper les complications potentielles lorsque la prise en charge initiale est insuffisante ou retardée. Chaque stade possède ses propres caractéristiques cliniques, son traitement spécifique et ses limites thérapeutiques à respecter.
L’Impaction du Sac Anal
L’impaction se définit par l’accumulation excessive d’un contenu épaissi ou desséché au sein d’un ou des deux sacs anaux. Les signes cliniques restent, à ce stade, relativement discrets : prurit périanal prédominant, érythème et desquamation secondaires au prurit dans les formes évoluées. Les sacs ne sont ni enflammés ni douloureux et s’expriment sans résistance notable à la palpation. Cette relative simplicité clinique contraste parfois avec la gêne fonctionnelle ressentie par l’animal, qui peut manifester une augmentation marquée du léchage ou du frottement au sol.
La prise en charge repose sur l’expression manuelle des sacs, geste simple mais dont le bénéfice reste limité s’il n’est pas accompagné de l’identification et du traitement de la cause sous-jacente. Les facteurs étiologiques à rechercher systématiquement incluent les anomalies diététiques, en particulier une alimentation à faible résidu fécal qui engendre des selles peu volumineuses et insuffisamment fermes pour assurer une pression mécanique efficace sur les sacs, les affections allergiques chroniques qui peuvent altérer la qualité et la quantité des sécrétions, et les épisodes répétés de diarrhée qui perturbent le mécanisme de vidange physiologique. L’antibiothérapie et l’analgésie ne sont pas indiquées à ce stade, leur prescription constituant une erreur thérapeutique par excès. Des expressions régulières programmées, associées à une correction diététique, suffisent généralement à contrôler l’impaction récidivante lorsque la cause prédisposante est correctement identifiée.
La Sacculite
La sacculite correspond à l’inflammation du sac anal, se présentant le plus souvent de façon unilatérale. L’évolution clinique suit un schéma caractéristique : d’abord prurigineux, le tableau se modifie progressivement pour devenir douloureux au fur et à mesure que l’inflammation s’intensifie. L’examen révèle un œdème périanal, un gonflement visible, un érythème marqué et des sacs dont le contenu est purulent ou hémorragique. La palpation des sacs est douloureuse, ce qui distingue nettement la sacculite de l’impaction simple et rend la manipulation de la région difficile chez un animal vigile non sédaté.
Le traitement de la sacculite repose sur l’expression des sacs sous sédation, la douleur rendant la manipulation impossible sans analgésie préalable, suivie d’un cathétérisme et d’un rinçage abondant du canal avec du sérum physiologique ou une solution antiseptique. Un protocole de rinçage intrasacculaire suivi d’une infusion d’une préparation commerciale associant corticoïde, antibiotique et antifongique, répété en moyenne deux à trois fois par animal, permet d’obtenir une résolution clinique dans la majorité des cas, sans recours à l’antibiothérapie systémique. L’application topique d’antiseptiques et d’antimicrobiens est recommandée, justifiée par la présence fréquente d’une pyodermite superficielle concomitante. Une analgésie systémique ou topique doit être prescrite pour assurer le confort de l’animal pendant la phase de résolution inflammatoire. Ce protocole doit être répété à intervalles bimensuels jusqu’à l’obtention d’une rémission clinique complète, définie par la disparition de l’inflammation tissulaire, de la douleur provoquée et du contenu anormal. La dermatite atopique représentant la comorbidité la plus fréquemment associée aux sacculites, sa recherche systématique doit s’intégrer au bilan de toute affection récidivante.
L’Abcès du Sac Anal
L’abcès représente le stade le plus avancé du processus inflammatoire. Il se caractérise par la fistulisation cutanée, parfois accompagnée d’hypothermie systémique dans les formes sévères. Un fait clinique contre-intuitif mérite d’être connu : la rupture de l’abcès s’accompagne souvent d’une diminution de la douleur perçue par l’animal, en raison de la décompression tissulaire qu’elle engendre. Ce soulagement apparent ne doit pas conduire à minimiser la gravité de la situation ni à différer la prise en charge, car la fistulisation marque une rupture de la barrière cutanée avec risque de dissémination bactérienne et de contamination des tissus profonds.
La prise en charge de l’abcès implique une incision au point de fluctuation maximal, suivie d’un écouvillonnage pour culture bactériologique et antibiogramme, geste indispensable pour guider une éventuelle antibiothérapie ciblée. Le rinçage, l’application topique d’antiseptiques et d’antimicrobiens, ainsi que l’utilisation d’anti-inflammatoires constituent le socle du traitement. L’antibiothérapie systémique n’est initiée qu’à réception des résultats de l’antibiogramme, les données cliniques montrent néanmoins que la résolution des lésions grâce aux seuls traitements topiques rend fréquemment son utilisation superflue. Cette approche, fondée sur l’antibiogramme plutôt que sur une antibiothérapie empirique systématique, s’inscrit dans les recommandations actuelles de bon usage des antibiotiques en médecine vétérinaire.
Néoplasies des Sacs Anaux : Un Diagnostic à Ne Pas Manquer
L’Adénocarcinome Apocrine du Sac Anal
Parmi les néoplasies malignes de la région périanale, l’adénocarcinome du sac anal occupe une place prépondérante, représentant 17 % des tumeurs malignes de cette région. Cette tumeur prend naissance dans les glandes apocrines de la paroi du sac anal. Elle touche préférentiellement les animaux d’âge avancé, le plus souvent au-delà de 9 ans. Contrairement à ce qui a longtemps été avancé dans la littérature ancienne, les études de grande cohorte n’ont pas mis en évidence de prédisposition sexuelle significative pour cette tumeur : aucun sexe ne présente de risque clairement supérieur à l’autre, et la vigilance diagnostique doit s’exercer de façon identique chez le mâle et chez la femelle. En revanche, des prédispositions raciales nettes sont documentées, le Cocker Anglais étant significativement sur-représenté avec un risque relatif moyen estimé à 7,3 par rapport aux chiens croisés. Son comportement biologique particulièrement agressif, combiné à la fréquence de sa découverte fortuite, en fait l’une des néoplasies vétérinaires qui justifient le plus impérieusement un examen rectal systématique à chaque consultation.
La présentation clinique est dominée par des signes souvent unilatéraux : gonflement périanal perceptible à la palpation, ténesme, dyschésie, saignements et comportements de léchage ou de traîneau accrus. Une atteinte bilatérale reste possible. Fait remarquable : une proportion substantielle de ces tumeurs est découverte fortuitement lors d’un examen clinique réalisé pour un autre motif, la masse demeurant asymptomatique au moment du diagnostic. Ce constat illustre la nécessité d’un examen systématique de la région périanale à chaque consultation, quelle qu’en soit l’indication initiale. Un animal consulté pour vaccination de routine, contrôle dentaire ou tout autre motif doit bénéficier d’une palpation rectale si son âge et son profil clinique le justifient.
Le Syndrome Paranéoplasique d’Hypercalcémie
L’adénocarcinome apocrine du sac anal possède la capacité de sécréter une protéine apparentée à l’hormone parathyroïdienne (PTHrP). Cette sécrétion ectopique induit un syndrome paranéoplasique d’hypercalcémie humorale, rapporté dans 25 à 90 % des cas selon les cohortes publiées, pouvant se manifester par une polyurie-polydipsie, une faiblesse musculaire, une constipation ou des troubles du rythme cardiaque. Ce syndrome se résout après exérèse complète de la tumeur, ce qui en fait à la fois un marqueur diagnostique et un critère de contrôle post-chirurgical. Dans certains cas, les signes systémiques liés à l’hypercalcémie peuvent précéder ou éclipser les signes locaux périanaux, ce qui peut conduire à un diagnostic différentiel initial orienté vers une hyperparathyroïdie primitive ou une autre cause d’hypercalcémie. La présence d’une hypercalcémie constitue par ailleurs un facteur de pronostic défavorable indépendant, en plus d’exposer à des risques anesthésiques et chirurgicaux accrus sur le plan cardiovasculaire et rénal. La mesure de la PTHrP sérique, associée au dosage de la PTH et à la calcémie totale et ionisée, permet de clarifier le tableau biologique.
Le dosage de la calcémie s’intègre donc obligatoirement dans le bilan préopératoire, au même titre que la biochimie complète, l’analyse d’urine et l’imagerie médicale visant à évaluer l’extension locale et à distance.
Potentiel Métastatique et Facteurs Pronostiques
Le taux de métastases de l’adénocarcinome apocrine du sac anal est élevé, y compris pour des tumeurs de taille modeste, ce qui en fait l’une des néoplasies vétérinaires les plus traîtres. La dissémination s’opère selon un schéma relativement prévisible : atteinte initiale des nœuds lymphatiques régionaux iliaques ou sacrés, puis dissémination secondaire aux poumons, au foie et à la rate en premier lieu, ainsi qu’aux os et à d’autres organes abdominaux dans les stades avancés. Des métastases au canal vertébral ont également été documentées. Le taux de métastases ganglionnaires à la présentation varie selon les cohortes de 26 % à plus de 90 %, selon les méthodes d’imagerie et les critères d’inclusion. Cette variabilité souligne que même les petites tumeurs ne sont pas exemptes de risque : environ 20 % des animaux présentant une tumeur primitive de moins de 2 cm ont déjà des métastases ganglionnaires au moment du diagnostic. Ce constat impose un bilan de stadification complet quel que soit le diamètre de la tumeur au moment de la découverte. L’échographie abdominale et la radiographie thoracique constituent les examens d’imagerie de première intention, tandis que la tomodensitométrie offre une sensibilité supérieure pour la détection de métastases ganglionnaires iliosacro-lombaires de petite taille, notamment pour les nœuds intrapelviens inaccessibles à l’échographie.
Sur le plan cytologique, la ponction à l’aiguille fine révèle un aspect neuroendocrinien caractéristique, avec des noyaux nus et une atypie polymorphe. Ce diagnostic cytologique doit être confirmé par l’histopathologie. Certains paramètres histologiques ont une valeur pronostique propre : un pattern de croissance solide, une infiltration périphérique marquée, la présence de nécrose et d’invasion lymphovasculaire sont associés à un pronostic défavorable. Le temps de survie médian varie considérablement selon le traitement instauré et le stade de la maladie. En l’absence de tout traitement, la survie médiane est de l’ordre de trois mois. La chirurgie seule permet d’atteindre une survie médiane de l’ordre d’un an, tandis que l’association de la chirurgie avec une chimiothérapie adjuvante ou une radiothérapie peut prolonger significativement cette survie, certaines stratégies multimodales étant associées à des durées supérieures à deux ans. Le pronostic est significativement amélioré lorsque la masse mesure moins de 2,5 cm au moment du diagnostic, en l’absence de métastases décelables, et lorsque l’exérèse des nœuds lymphatiques régionaux est réalisée conjointement à l’exérèse tumorale. Ces éléments pronostiques soulignent l’importance d’un dépistage précoce et d’une chirurgie complète et bien planifiée. La radiothérapie stéréotaxique corporelle (SBRT) représente une option thérapeutique validée pour le traitement des nœuds lymphatiques métastatiques iliosacro-lombaires lorsque la résection chirurgicale est déclinée ou impossible, avec des taux de contrôle local élevés et une survie médiane comparable aux approches chirurgicales dans les séries récentes.
Autres Néoplasies de la Région des Sacs Anaux
Le carcinome épidermoïde des glandes du sac anal, bien que rare, constitue une affection grave supplémentaire. Son comportement local agressif et son potentiel métastatique en font une entité à ne pas négliger face à toute lésion périanale atypique. Parmi les autres néoplasies moins fréquentes touchant la région périanale au sens large, on recense les adénomes apocrines, les tumeurs mésenchymateuses diverses et les mastocytomes. Ce dernier, en particulier, peut se présenter de façon cliniquement anodine dans cette localisation, ce qui justifie le recours systématique à la ponction à l’aiguille fine devant toute lésion nodulaire périanale. Chacune de ces entités requiert une démarche diagnostique cytologique ou histologique pour être correctement caractérisée et prise en charge.
Affections Périanales Indépendantes des Sacs Anaux
Érythème et Prurit Périanal : Penser Allergie
Un érythème prurigineux localisé à la zone périanale ou étendu à l’ensemble du périnée représente l’une des manifestations cliniques les plus fréquentes en dermatologie vétérinaire. Dans ce contexte, les maladies allergiques tiennent le rôle de premier plan : dermatite par allergie aux piqûres de puces (DAPP), allergie alimentaire et dermatite atopique se partagent la causalité. Ce signe clinique peut, dans certains cas, constituer la seule manifestation visible de la maladie allergique, sans aucune atteinte cutanée généralisée associée. Un chien présentant un érythème périanal isolé, sans aucune autre lésion cutanée identifiable, doit donc bénéficier d’une investigation allergologique complète et non d’un simple traitement local symptomatique.
Le diagnostic différentiel intègre les infestations parasitaires, puces, parasites intestinaux tels que les Dipylidium ou les ankylostomes, et les surinfections à Malassezia, levures dont la prolifération est souvent secondaire à un terrain allergique. La démarche diagnostique progresse par exclusion méthodique : les causes infectieuses et parasitaires sont écartées en premier lieu, avant d’engager une investigation allergologique, incluant un régime d’éviction alimentaire strict lorsque l’allergie alimentaire est suspectée. L’errance diagnostique fréquemment observée dans ces cas résulte souvent d’une investigation incomplète ou d’un régime d’éviction mal conduit, ce qui souligne l’importance d’une démarche structurée et méthodique.
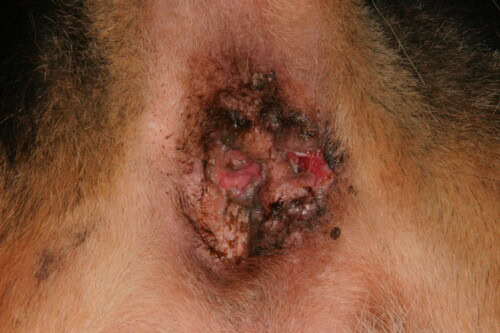
La Fistule Périanale Canine : Une Maladie Immuno-Médiée Chronique
La fistule périanale canine, également nommée furonculose anale, représente l’une des affections périanales les plus sévères et les plus délicates à gérer. Elle s’intègre dans le cadre des maladies inflammatoires chroniques d’origine immunitaire, portée par un mécanisme d’inflammation médiée par les lymphocytes T, associé à un défaut de cicatrisation tissulaire. Ce défaut de cicatrisation constitue un facteur aggravant majeur, car il entretient l’ouverture des trajets fistuleux et compromet la résolution spontanée des lésions, même en l’absence de surinfection bactérienne active. Le Berger Allemand représente plus de 80 % des cas rapportés dans la littérature, ce qui traduit une composante génétique forte dans la susceptibilité à la maladie. D’autres races peuvent être concernées, notamment les Retrievers et certaines races à queue large et basse portée qui favorisent un microenvironnement humide et peu aéré autour de l’anus.
Les bases immunopathologiques de la maladie sont mieux caractérisées aujourd’hui. Des variations alléliques ont été identifiées chez les Bergers Allemands atteints. L’analyse histopathologique des lésions révèle un infiltrat cellulaire mononucléé dominé par des lymphocytes T CD3+ avec un profil cytokinique compatible avec une réponse de type Th1, marqué notamment par une augmentation de l’expression des ARNm d’IL-2 et d’IFN-γ dans les tissus lésionnels. Une surexpression des métalloprotéinases matricielles MMP-9 et MMP-13 dans la peau lésionnelle explique le défaut de cicatrisation tissulaire qui entretient les trajets fistuleux. Une dysfonction du récepteur NOD2, impliqué dans la reconnaissance des motifs moléculaires associés aux pathogènes bactériens, a également été proposée comme mécanisme contributif. Par ailleurs, une dysbiose significative du microbiote cutané et rectal a été documentée chez les Bergers Allemands atteints, avec des différences de composition significatives par rapport aux chiens sains. Cette dysbiose se modifie au cours de la résolution des lésions sous traitement immunomodulateur, ouvrant des perspectives sur le rôle potentiel du microbiome dans la pathogenèse de la maladie. L’ensemble de ces données place la fistule périanale canine comme modèle animal spontané de la maladie de Crohn fistulisante chez l’homme, avec laquelle elle partage des bases génétiques et immunopathologiques.
Fistules périanales modérées
Présentation Clinique
La maladie se caractérise morphologiquement par des trajets fistuleux multiples et des ulcères de taille très variable, allant de lésions millimétriques discrètes à des ulcérations massives délabrantes. La distribution typiquement circonférentielle de ces lésions autour de l’anus constitue un élément sémiologique discriminant, permettant de la distinguer des atteintes focalisées des sacs anaux. Cette distribution circonférentielle reflète l’atteinte diffuse de la zone cutanée périanale et non une lésion focale liée à l’obstruction d’un sac. Les signes cliniques fonctionnels comprennent le léchage et le frottement compulsifs, une dyschésie douloureuse pouvant aboutir à de l’anorexie comportementale, l’animal refusant de s’alimenter par anticipation de la douleur liée à la défécation,, ainsi que la présence de sang et d’exsudats autour de la région anale.
Une atteinte concomitante des sacs anaux ou du rectum reste possible et doit être activement recherchée lorsque la réponse thérapeutique s’avère insuffisante. L’exploration endoscopique peut alors s’avérer nécessaire pour évaluer l’étendue de l’atteinte muqueuse rectale et guider la décision thérapeutique. Une colite concomitante a été rapportée dans certains cas, suggérant un continuum entre la fistule périanale canine et les maladies inflammatoires chroniques de l’intestin, à l’instar de ce qui est observé dans la maladie de Crohn chez l’homme. Par ailleurs, une association entre réactivité alimentaire et fistule périanale a été documentée chez le Berger Allemand, justifiant d’associer un régime d’éviction alimentaire au traitement immunomodulateur lors de rechutes fréquentes malgré une immunosuppression bien conduite.
Prise en Charge Thérapeutique
Un point fondamental doit être gravé dans la pratique clinique : les antibiotiques sont inefficaces sur l’évolution de la maladie de fond. Leur utilisation isolée ou prolongée ne modifie pas le processus immuno-médié sous-jacent, inflammation lymphocytaire T, surexpression de MMP-9 et MMP-13, défaut de cicatrisation, et expose au risque de résistances bactériennes. Ce point est d’autant plus important que la fistule périanale canine est une maladie à rechute fréquente, et qu’une antibiothérapie empirique répétée lors de chaque récidive constitue une dérive thérapeutique préjudiciable à long terme. Le traitement de référence repose sur les immunomodulateurs. La ciclosporine per os constitue la molécule de première intention, avec un niveau de preuve élevé : administrée jusqu’à l’obtention d’une rémission clinique, sa dose est ensuite progressivement réduite au seuil minimal efficace. L’association ciclosporine et kétoconazole représente une stratégie pharmacologique validée qui permet, par inhibition enzymatique hépatique, d’augmenter la biodisponibilité de la ciclosporine et de réduire de plus de 80 à 90 % la dose nécessaire pour atteindre les concentrations sanguines thérapeutiques. Cette combinaison réduit significativement le coût du traitement dans les pays où le kétoconazole est peu cher, ce qui n’est pas le cas de la France, sans compromettre l’efficacité et doit être envisagée en première intention lorsque le budget du propriétaire est une contrainte. En cas d’échec de la ciclosporine seule, la stratégie de deuxième ligne recommandée par la revue de littérature la plus récente est la combinaison prednisolone systémique et tacrolimus topique, et non le tacrolimus seul. Le tacrolimus en application topique représente une alternative locale efficace, particulièrement adaptée aux lésions de taille modérée lorsqu’il est utilisé dans ce cadre combiné. A noter que l’utilisation de tacrolimus en topique est interdite dans certains pays, comme la France. Les vétérinaires français ne peuvent donc légalement ni prescrire ni se procurer ce médicament.
D’autres options thérapeutiques ont été rapportées dans la littérature avec des niveaux de preuves variables : corticoïdes, azathioprine, oclacitinib, mycophénolate mofétil, thérapie par lumière fluorescente et modifications diététiques. Ces dernières méritent une attention particulière, une composante alimentaire prédisposante étant suspectée dans certains cas, ce qui conduit certains cliniciens à associer un régime d’éviction à l’immunomodulation. L’oclacitinib, inhibiteur de la voie JAK-STAT impliquée dans la signalisation des interleukines pro-inflammatoires, représente une piste thérapeutique prometteuse dont l’évaluation clinique a donné des résultats favorables dans des cas résistants à la ciclosporine. La thérapie par lumière fluorescente (photobiomodulation), par ses effets anti-inflammatoires et biostimulants sur la cicatrisation tissulaire, constitue également un outil adjuvant intéressant, notamment pour favoriser la fermeture des trajets fistuleux résistants. Les thérapies cellulaires à base de cellules souches mésenchymateuses représentent une voie expérimentale en cours d’exploration.
Les Tumeurs des Glandes Hépatoïdes : Une Entité à Part Entière
Les glandes hépatoïdes, dénomination tirée de la ressemblance histologique de leurs cellules avec les hépatocytes, sont des glandes sébacées modifiées, circonscrites à la zone cutanée périanale. Les tumeurs qui en sont issues représentent collectivement 25 % de l’ensemble des tumeurs cutanées canines, ce qui en fait un groupe néoplasique quantitativement majeur et l’un des plus fréquemment rencontrés en oncologie dermatologique vétérinaire.
Adénome Hépatoïde
L’adénome hépatoïde est la forme la plus fréquente, apparaissant sous forme solitaire ou multiple, avec une prédilection marquée pour les mâles entiers d’âge moyen à avancé. Cette prédisposition sexuelle traduit une pathogénie hormono-dépendante, les androgènes jouant un rôle trophique sur ces glandes. Une hyperplasie nodulaire périanale des glandes hépatoïdes, observée chez des mâles entiers d’âge moyen, peut précéder le développement d’un adénome véritable ; cette hyperplasie nodulaire bénigne constitue également une indication à la castration. Le diagnostic est établi sur la base de l’examen clinique, masse sessile ou pédiculée, charnue, à surface parfois ulcérée, et confirmé par la cytologie ou l’histologie. La cytologie préchirurgicale apporte des informations utiles pour guider la décision opératoire : plusieurs critères cytologiques permettent de distinguer les lésions bénignes des lésions malignes avec une précision diagnostique satisfaisante, sans toutefois se substituer à l’examen histopathologique.
Le traitement curatif associe systématiquement l’excision chirurgicale complète de la masse et la castration, chirurgicale ou chimique, cette dernière étant indispensable pour prévenir les récidives tumorales liées à la stimulation androgénique résiduelle. La castration seule peut induire une régression partielle de certains adénomes hépatoïdes, mais l’excision chirurgicale reste le traitement de référence pour éliminer la lésion en place et obtenir un diagnostic histologique définitif. Le pronostic est excellent, les métastases restant exceptionnellement rares pour l’adénome. Ce pronostic favorable contraste avec celui de l’adénocarcinome hépatoïde et souligne l’importance d’une caractérisation histologique précise pour orienter correctement la prise en charge.
Adénocarcinome Hépatoïde
L’adénocarcinome hépatoïde est d’occurrence sensiblement plus rare. Son comportement biologique plus agressif se traduit par un potentiel d’invasion locale plus marqué et un risque métastatique supérieur à celui de l’adénome. Cette différence de comportement impose une démarche diagnostique et chirurgicale plus rigoureuse, avec un bilan d’extension approprié, incluant imagerie abdominale et thoracique, avant toute décision opératoire. La distinction histologique entre adénome et adénocarcinome hépatoïde peut s’avérer délicate dans certains cas et requiert l’expertise d’un anatomopathologiste vétérinaire expérimenté. Des systèmes de grading histologique ont été proposés pour affiner la stratification pronostique au-delà de la seule dichotomie bénin/malin, en intégrant des critères architecturaux et cytologiques susceptibles de prédire l’évolution clinique.
Dermatoses de la Région Périnéale
Le Cadre Diagnostique : Anamnèse et Chronologie
La région périnéale, de par sa localisation anatomique entre l’anus et les organes génitaux, subit une exposition chronique aux matières fécales, à l’urine et à divers agents irritants. Les races à faible densité pilleuse périnéale sont particulièrement prédisposées aux dermatoses de cette zone. Face à une lésion périnéale, l’approche diagnostique repose sur une anamnèse précise permettant de déterminer la chronologie d’apparition et d’évolution des lésions. Trois cadres cliniques se distinguent nettement : la présentation aiguë, la présentation chronique et la présentation nodulaire, chacune orientant vers un spectre étiologique distinct et requérant une stratégie diagnostique adaptée.
Présentation Aiguë : L’Irritation Comme Facteur Déclenchant
Une présentation aiguë s’inscrit typiquement dans le contexte d’un épisode de diarrhée ou d’incontinence fécale ou urinaire récent. L’examen clinique révèle une peau érythémateuse, humide, avec une exsudation variable. Le diagnostic différentiel principal oriente vers une dermatite de contact irritative, les enzymes digestives contenues dans les selles diarrhéiques constituant le principal agent lésionnel, dont la protéase et les sels biliaires exercent une action directement corrosive sur l’épiderme périnéal, et vers les escarres de décubitus dans les cas d’immobilité prolongée. Une surinfection bactérienne secondaire doit toujours être recherchée par cytologie, les érythèmes exsudatifs constituant un terrain favorable à la prolifération de coques et de bacilles.
Présentation Chronique : Le Terrain Allergique Dominant
Dans sa forme chronique, la dermatose périnéale se manifeste par un prurit et un léchage persistants. Les lésions évoluées présentent un tableau cutané caractéristique : érythème, alopécie de friction, hyperpigmentation, lichénification et séborrhée marquée. Ces modifications témoignent d’un remodelage cutané chronique lié au prurit auto-entretenu, dans lequel le grattage et le léchage répétés altèrent la barrière cutanée et favorisent la pénétration d’allergènes et d’agents infectieux. Ce cercle vicieux prurit-lésion-prurit est au cœur de la physiopathologie de la dermatite allergique chronique.
Le diagnostic différentiel s’oriente principalement vers une dermatite allergique sous-jacente, atopique, alimentaire ou liée aux piqûres de puces, fréquemment compliquée de pyodermite bactérienne ou de dermatite à Malassezia. Ces surinfections secondaires participent à l’entretien du cycle prurit-grattage-lésion et doivent être traitées en parallèle de la cause primaire. Une démarche diagnostique qui traiterait uniquement les infections secondaires sans identifier et contrôler la maladie allergique sous-jacente est vouée à l’échec et entraîne des rechutes fréquentes.
Présentation Nodulaire : Néoplasies et Granulomes en Priorité
Des lésions périnéales nodulaires à croissance progressive, initialement non prurigineuses, constituent une présentation clinique nécessitant une investigation cytologique ou histologique rapide. Le diagnostic différentiel doit inclure les néoplasies cutanées diverses, les nodules infectieux, fistules bactériennes profondes ou mycosiques, et les granulomes parasitaires. La ponction à l’aiguille fine représente le premier geste diagnostique recommandé devant toute lésion nodulaire périanale ou périnéale. Ce geste simple, réalisable en consultation sans sédation dans la plupart des cas, permet d’orienter rapidement vers une nature inflammatoire, infectieuse ou néoplasique et de planifier la suite de la prise en charge en conséquence. La biopsie avec examen histopathologique reste indispensable lorsque le résultat cytologique est non concluant ou lorsqu’une caractérisation tissulaire précise est nécessaire pour décider du traitement.
Affections Périgénitales : Spécificités par Sexe
Chez la Femelle : L’Intertrigo Vulvaire
L’intertrigo vulvaire est une affection dermatologique fréquente chez la chienne, particulièrement observée en présence de deux facteurs prédisposants majeurs : l’obésité et la vulve hypoplasique. Dans ces configurations anatomiques, les replis cutanés périvulvaires créent un microenvironnement chaud, humide et macéré, propice à l’accumulation de sécrétions, sécrétions vaginales, urine résiduelle, débris cellulaires. Cette accumulation favorise le développement de réactions inflammatoires locales, d’érosions et de surinfections bactériennes ou fongiques secondaires. Les agents pathogènes les plus fréquemment impliqués dans les surinfections de l’intertrigo vulvaire incluent les bactéries gram-positives telles que les staphylocoques, et les levures de type Malassezia. Les signes cliniques associent érythème périvulvaire, exsudation, prurit local et parfois odeur nauséabonde. La prise en charge associe idéalement le traitement local de l’infection et la correction, lorsque possible, du facteur prédisposant anatomique ou pondéral. La chirurgie périvulvaire, épisio-plastie ou vulvoplastie, peut être envisagée pour corriger anatomiquement les replis excessifs chez les chiennes présentant une vulve hypoplasique sévère et des récidives fréquentes malgré une prise en charge médicale bien conduite.
Intertrigo vulvaire
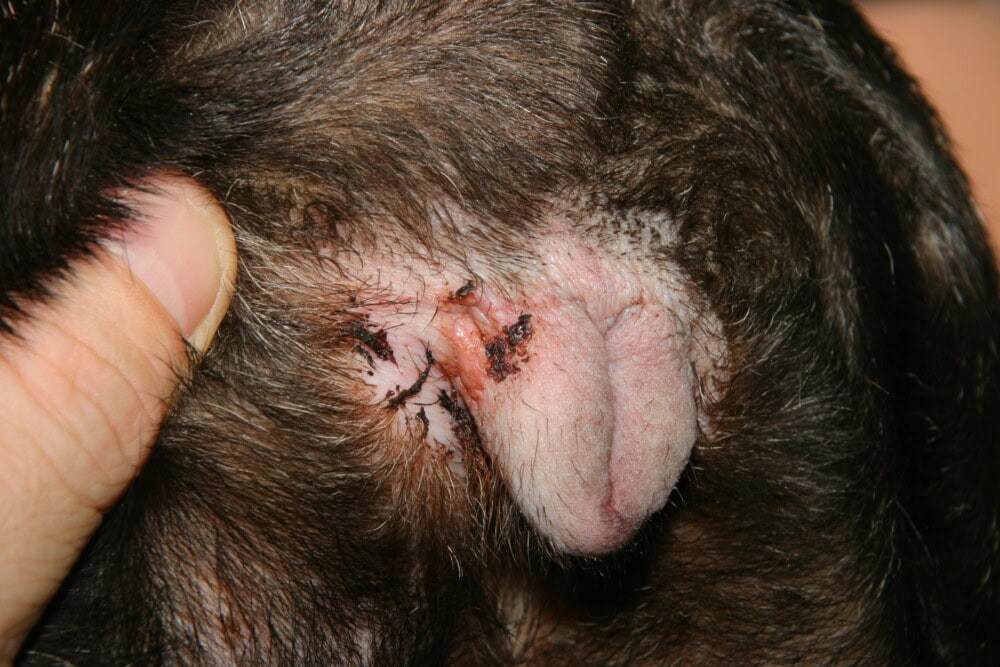
Chez le Mâle : La Dermatite Scrotale
Le scrotum, de par la finesse et la sensibilité de son épiderme, représente une zone de prédilection pour les réactions dermatologiques inflammatoires chez le chien mâle. La finesse particulière de l’épiderme scrotal, associée à son exposition directe à l’environnement, le rend hautement réactif aux stimuli allergiques, irritants et infectieux. La dermatite scrotale est fréquemment observée, avec un spectre étiologique comprenant les réactions allergiques, atopie, allergie de contact, les infections bactériennes et la dermatite à Malassezia. Le contact avec des substrats irritants, des produits ménagers ou des surfaces rugueuses peut également déclencher ou aggraver ce tableau, notamment chez des animaux en contact prolongé avec des surfaces traitées chimiquement. La cytologie cutanée oriente rapidement vers le ou les agents pathogènes impliqués et guide le traitement topique. Une dermatite scrotale récidivante doit systématiquement faire évoquer une dermatite atopique sous-jacente, dont elle peut constituer l’une des manifestations cliniques predominantes.
Tumeurs Périgénitales
Les tumeurs affectant la région périgénitale restent moins fréquentes que celles de la région périanale, mais méritent d’être considérées dans le diagnostic différentiel de toute masse périgénitale à croissance progressive. Parmi les néoplasies périgénitales rencontrées chez le chien, on peut citer les tumeurs vénériennes transmissibles, les carcinomes épidermoïdes et diverses tumeurs mésenchymateuses. La tumeur vénérienne transmissible, bien qu’encore peu fréquente en Europe occidentale, doit figurer dans le diagnostic différentiel des masses périgénitales chez les chiens avec antécédents de déplacements dans des zones d’enzootie. Le traitement chirurgical constitue généralement la première intention thérapeutique pour les tumeurs périgénitales bénignes ou localisées, tandis que les formes malignes peuvent nécessiter une approche combinée associant chirurgie, chimiothérapie ou radiothérapie selon l’histotype et le stade.
Synthèse
La prise en charge des affections dermatologiques périanales, périnéales et périgénitales chez le chien repose sur une démarche clinique rigoureuse, articulée autour de trois axes complémentaires. Premièrement, la connaissance précise de l’anatomie régionale, qui conditionne la reconnaissance des structures impliquées et l’interprétation des lésions observées. Deuxièmement, une sémiologie fine distinguant les affections aiguës des affections chroniques, les tableaux prurigineux des tableaux douloureux, et les atteintes des sacs anaux des dermatoses cutanées indépendantes. Troisièmement, un recours raisonné aux examens complémentaires, cytologie, culture bactériologique orientée, imagerie, bilan biochimique, dont la valeur diagnostique est à interpréter dans le contexte clinique et non de façon isolée.
L’approche algorithmique fondée sur la chronologie des lésions, aiguë ou chronique constitue un outil structurant particulièrement précieux pour le praticien confronté à la diversité des présentations cliniques périnéales. Cette approche permet de hiérarchiser le diagnostic différentiel, de sélectionner les examens complémentaires les plus pertinents et d’éviter des investigations inutiles ou des traitements empiriques non ciblés.
Deux enseignements transversaux méritent d’être particulièrement retenus. D’une part, la culture bactériologique systématique du contenu des sacs anaux ne constitue pas un outil diagnostique fiable en l’absence de contexte clinique d’abcès avéré, en raison de la présence habituelle de micro-organismes dans ce compartiment chez les animaux sains. D’autre part, l’antibiothérapie systémique doit être réservée aux situations où elle est réellement justifiée, abcès avec antibiogramme , surinfection documentée, et ne doit en aucun cas constituer un traitement empirique de première intention pour des tableaux inflammatoires non compliqués.
Les perspectives de recherche dans ce domaine concernent notamment la compréhension des mécanismes immunopathologiques précis de la fistule périanale canine, dont la complexité reste partiellement élucidée, notamment le rôle du microbiote péri-anal comme facteur potentiellement modifiable par le traitement, ainsi que l’identification de biomarqueurs prédictifs de récidive pour les tumeurs hépatoïdes. L’évaluation prospective de nouvelles molécules immunomodulatrices, comme les inhibiteurs de JAK appliqués à la fistule périanale, ouvre des pistes thérapeutiques prometteuses qui mériteront d’être documentées par des essais cliniques contrôlés. Par ailleurs, l’amélioration des techniques de stadification préopératoire pour l’adénocarcinome apocrine du sac anal, notamment par le recours systématique à la tomodensitométrie et le développement de marqueurs moléculaires prédictifs du potentiel métastatique, ainsi que l’évaluation de la radiothérapie stéréotaxique corporelle dans le traitement multimodal, constituent des axes de recherche actifs susceptibles d’améliorer significativement le pronostic de cette tumeur.
Conclusion
Les régions périanale, périnéale et périgénitale concentrent, dans un territoire anatomique restreint, une diversité remarquable d’affections dermatologiques dont les étiologies, les mécanismes et les traitements diffèrent fondamentalement. Ces régions jouent un rôle important dans la communication sociale canine, ce qui justifie pleinement l’attention clinique qui leur est portée au-delà de leur seule importance médicale. L’examen rectal systématique, l’analyse rigoureuse de la chronologie des lésions, et la cytologie réalisée à bon escient permettent d’orienter le diagnostic avec précision. La distinction entre affection fonctionnelle des sacs anaux, processus inflammatoire immuno-médié, dermatose allergique et néoplasie conditionne directement l’efficacité de la prise en charge thérapeutique. Ignorer cette région ou la réduire à un examen superficiel expose à des retards diagnostiques aux conséquences cliniques parfois graves, notamment dans le cas de l’adénocarcinome apocrine du sac anal, une tumeur sans prédisposition sexuelle établie, touchant l’ensemble des animaux d’âge avancé quelle que soit leur appartenance sexuelle, et dont le potentiel métastatique élevé rend chaque semaine de retard diagnostique potentiellement préjudiciable au pronostic.
Maina E. From perianal to perigenital conditions in dogs. Programme pratique du 35th European Veterinary Dermatology Congress. Bilbao, Spain ; 11-13 september 2025.