La dermatite atopique canine affecte 10 à 15 % de la population canine mondiale et constitue l’un des premiers motifs de consultation en dermatologie vétérinaire. Face à ce fléau, de nouveaux traitements émergent avec un excellent rapport bénéfice/risque. Tour d’horizon complet sur Zenrelia (ilunocitinib) qui est le premier des nouveaux inhibiteurs des Janus Kinase à avoir été commercialisé après l’oclacitinib (Apoquel).
William BORDEAU, DVM
Cabinet VetDerm, Maisons Alfort (94)
Février 2026
PARTIE I — INTRODUCTION ET CONTEXTE
1.1 La dermatite atopique canine : cadre nosologique
1.1.1 Définition et physiopathologie
La dermatite atopique canine (DAC) est une dermatose inflammatoire chronique à prédisposition génétique, caractérisée par un prurit récurrent et des lésions cutanées érythémateuses associées à une sensibilisation vis-à-vis d’allergènes environnementaux (Hensel 2015). La physiopathologie de la DAC repose sur trois piliers intriqués : une dysfonction de la barrière cutanée, une dysrégulation immunitaire et une sensibilisation allergénique progressive. La barrière épidermique est altérée par des anomalies structurelles du stratum corneum, comparables à celles décrites dans la dermatite atopique humaine où la mutation du gène de la filaggrine est documentée. Chez le chien, les études ont mis en évidence des anomalies d’expression de protéines de jonction intercellulaire (claudines, occludine) dans les biopsies cutanées lésionnelles de chiens atopiques (Marsella 2021). Cette altération de la barrière facilite la pénétration transcutanée des allergènes et des micro-organismes, entretenant une stimulation antigénique chronique.
Sur le plan immunologique, la DAC se caractérise par une polarisation initiale de type Th2 avec surexpression des interleukines IL-4, IL-5, IL-13 et IL-31, suivie d’une phase chronique où coexistent des réponses Th1 (interféron-gamma, IFN-γ) et Th17 (Pucheu-Haston 2015). L’IL-31, cytokine pruritogène majeure, se lie à son récepteur hétérodimérique (IL-31RA/OSMR) exprimé sur les neurones sensitifs cutanés et active la voie de signalisation JAK1/JAK2-STAT3, générant le signal de démangeaison transmis aux centres nerveux supérieurs (Gonzales 2013). Des élévations significatives des concentrations circulantes d’IL-31, d’IL-17 et d’IgE totales ont été documentées chez les chiens atopiques par rapport aux témoins sains (Chaudhary 2019). La thymic stromal lymphopoietin (TSLP) et la substance P participent à l’amplification de cette cascade pruritogène. Le rôle du microbiome cutané, avec une prolifération de Staphylococcus pseudintermedius dans les sites lésionnels, constitue un facteur aggravant documenté qui entretient la boucle inflammatoire par activation des récepteurs Toll-like (TLR-2) kératinocytaires (Santoro 2015).
1.1.2 Épidémiologie et prédispositions raciales
La prévalence de la DAC est estimée entre 10 et 15 % de la population canine globale, avec des variations régionales liées aux conditions environnementales et aux pratiques d’élevage (Hillier 2001). Environ 17 millions de chiens souffrent de maladies cutanées allergiques aux États-Unis, incluant la DAC, les allergies alimentaires et la dermatite par allergie aux piqûres de puces (Drechsler 2024). La DAC constitue l’un des premiers motifs de consultation en dermatologie vétérinaire et représente un fardeau économique considérable pour les propriétaires, avec des coûts annuels de traitement estimés entre 500 et 2 000 euros par animal, selon le pays, le protocole thérapeutique et la sévérité.
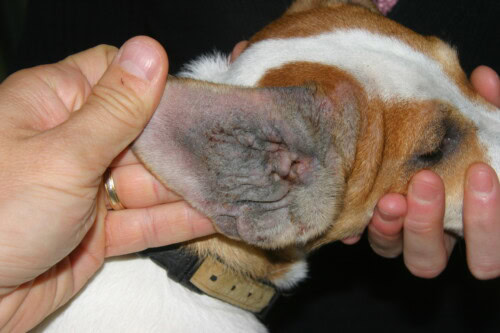
Plusieurs races présentent une prédisposition génétique bien documentée. Le Labrador Retriever manifeste un phénotype clinique dominé par un prurit érythémateux bilatéral et symétrique des espaces interdigités palmaires et plantaires, des pavillons auriculaires et des plis axillaires, avec des otites externes cérumineuses récidivantes et des pododermatites chroniques. Le West Highland White Terrier développe une forme précoce et sévère de DAC, avec une prévalence élevée dans certaines lignées, caractérisée par un érythème facial, périoculaire et périlabial intense, associé à une lichénification rapide des zones de flexion (Favrot 2020). Le Bouledogue Français présente des manifestations cliniques à tropisme inguinal, périnéal et interdigité, avec une fréquence accrue de surinfections bactériennes et fongiques (Malassezia pachydermatis) nécessitant des traitements anti-infectieux concomitants. Le Golden Retriever, le Boxer, le Shar Pei et le Berger Allemand figurent parmi les autres races à risque élevé (Hensel 2015). Le Shar Pei mérite une mention particulière : la sévérité de la DAC dans cette race est corrélée à la mucine dermique excessive, qui altère la thermorégulation cutanée et favorise la macération dans les plis, créant un environnement propice aux surinfections. Le Boxer présente un profil clinique particulier avec une prédominance d’atteinte abdominale ventrale et inguinale, une lichénification précoce et une propension aux otites prolifératives. Aucun gène de susceptibilité spécifique à la DAC n’a été formellement identifié chez le chien, à la différence de l’ichthyose du Golden Retriever (mutation PNPLA1).
Le Jack Russell est l’une des nombreuses races prédisposées par la Dermatite Atopique canine
1.2 Les options thérapeutiques disponibles avant l’ilunocitinib
1.2.1 Glucocorticoïdes
Les glucocorticoïdes systémiques (prednisolone, méthylprednisolone) ont longtemps constitué le traitement de première intention de la DAC en raison de leur efficacité rapide sur le prurit et l’inflammation. La prednisolone procure une réduction du prurit supérieure à 50 % chez environ 70 % des chiens dès les 48 premières heures (Olivry 2015). Toutefois, l’utilisation prolongée expose à des effets indésirables systémiques bien caractérisés : polyuro-polydipsie, polyphagie, prise de poids, atrophie cutanée, calcinose, diabète sucré iatrogène, susceptibilité accrue aux infections urinaires et cutanées, et suppression de l’axe hypothalamo-hypophyso-surrénalien.
1.2.2 Ciclosporine
La ciclosporine, inhibiteur de la calcineurine, constitue la première molécule immunomodulatrice à avoir obtenu une autorisation de mise sur le marché spécifique pour la DAC. À la posologie de 5 mg/kg/jour per os, elle réduit le prurit de 50 % chez environ 65 % des chiens après 4 à 6 semaines de traitement (Steffan 2006). Son délai d’action prolongé (4 à 6 semaines pour atteindre l’efficacité maximale) et la fréquence des effets digestifs (vomissements chez 25 à 30 % des animaux en début de traitement) limitent l’observance thérapeutique.
1.2.3 Oclacitinib
L’oclacitinib (APOQUEL, Laboratoire Zoetis), premier inhibiteur de JAK commercialisé en médecine vétérinaire en 2013, a constitué une avancée thérapeutique majeure. Cet inhibiteur préférentiel de JAK1 et JAK3 inhibe la signalisation de l’IL-31, de l’IL-4 et de l’IL-13, procurant une réduction rapide du prurit dès 4 heures après administration (Gonzales 2014). La posologie recommandée est de 0,4-0,6 mg/kg deux fois par jour pendant 14 jours (phase d’induction), puis une fois par jour en traitement d’entretien. L’étude de Cosgrove et al. (Cosgrove 2015) a documenté une efficacité et une tolérance satisfaisantes sur 630 jours d’utilisation continue. Toutefois, le passage d’une administration biquotidienne à une administration quotidienne en phase d’entretien expose à un phénomène de rebond du prurit entre J14 et J28, documenté par Fukuyama et al. (2017) et par Olivry et al. (2023).
1.2.4 Lokivetmab
Le lokivetmab (CYTOPOINT, Laboratoire Zoetis), anticorps monoclonal caninisé anti-IL-31, représente la première biothérapie ciblée en dermatologie vétérinaire. Administré par injection sous-cutanée à la dose minimale de 1 mg/kg à 2 mg/kg toutes les 4 à 8 semaines. L’essai dose-réponse initial (Michels 2016) a évalué des doses de 0,125 à 2 mg/kg. Il neutralise spécifiquement l’IL-31 circulante et procure un soulagement du prurit chez environ 70 % des chiens traités (Michels 2016). Son mode d’action purement antiprurigineux, sans activité anti-inflammatoire directe sur les lésions cutanées, et la nécessité d’injections mensuelles en clinique constituent ses limites. La combinaison lokivetmab-oclacitinib a été décrite dans la littérature pour les cas réfractaires.
1.3 Historique du développement et enregistrement réglementaire
1.3.1 Développement préclinique et réglementaire
L’ilunocitinib a été développé par Elanco Animal Health comme nouvelle entité moléculaire de la classe des inhibiteurs de JAK, spécifiquement conçue pour l’utilisation vétérinaire dans le traitement du prurit associé aux dermatites allergiques canines. Le brevet principal décrit la molécule comme le composé 27 d’une série de dérivés azétidine et cyclobutane actifs sur les Janus kinases, avec une expiration prévue en 2040 (brevet US 11548895). Le programme de développement clinique a comporté des études de sécurité sur espèce cible (Kuntz 2025), des études pharmacocinétiques (Boerngen 2026), trois essais cliniques de terrain (Forster 2025a, 2025b, 2025c) et deux études de réponse vaccinale (Fent 2025a, Fent 2025b).
1.3.2 Autorisations de mise sur le marché
L’autorisation de mise sur le marché initiale a été délivrée par la Food and Drug Administration (FDA) américaine le 19 septembre 2024 pour le contrôle du prurit associé aux dermatites allergiques et le contrôle de la dermatite atopique chez le chien âgé d’au moins 12 mois. Le lancement commercial aux États-Unis a suivi immédiatement cette approbation. Par la suite, l’autorisation a été étendue au Brésil, au Canada (décembre 2024) et au Japon au cours du premier semestre 2025. En Europe, le Comité des médicaments à usage vétérinaire de l’Agence européenne des médicaments (EMA) a adopté un avis positif en juin 2025, et l’autorisation de mise sur le marché européenne a été délivrée par la Commission européenne en juillet 2025, avec un lancement commercial immédiat. En France, le médicament vétérinaire ZENRELIA est disponible sur prescription vétérinaire depuis le troisième trimestre 2025. En septembre 2025, la FDA a approuvé une mise à jour du RCP américain, retirant la mention de « maladie vaccinale fatale induite » de l’étiquetage, sur la base de données scientifiques complémentaires démontrant que les cas d’hépatite adénovirale observés lors de l’étude vaccinale initiale résultaient d’une infection naturelle par le CAV-1, et non d’une maladie vaccinale induite (Fent 2025a). Plus de 800 000 chiens ont été traités dans le monde depuis le lancement, selon les données communiquées par Elanco fin 2025.
PARTIE II — CHIMIE ET STRUCTURE MOLÉCULAIRE
2.1 Identité chimique et propriétés physicochimiques
2.1.1 Structure moléculaire
La dénomination commune internationale de la molécule est ilunocitinib. Le nom de marque est Zenrelia (Elanco). La formule moléculaire brute est C₁₇H₁₇N₇O₂S, correspondant à une masse molaire exacte de 383,12 Da et une masse moléculaire de 383,43 g/mol. L’ilunocitinib appartient à la famille des pyrrolopyrimidines avec des groupes fonctionnels azétidine et sulfonamide, structurellement distinct de l’oclacitinib, autre pyrrolopyrimidine mais portant un groupement cyclohexylamine trans-substitué et un méthanesulfonamide N-méthylé. L’ilunocitinib partage avec le baricitinib un mécanisme d’action commun (inhibition compétitive du site ATP des JAK) et un profil de sélectivité isoforme partiellement chevauchant (JAK1/JAK2), mais appartient à une famille chimique structurellement distincte. (Clark 2014). La configuration tridimensionnelle de l’ilunocitinib lui confère une occupation du site catalytique ATP-dépendant des kinases JAK1, JAK2 et TYK2, avec une affinité différentielle selon les isoformes.
2.1.2 Propriétés physicochimiques
L’ilunocitinib présente une faible solubilité aqueuse, facteur limitant de l’absorption à forte dose, et une perméabilité modérée à élevée dans le modèle cellulaire Caco-2, avec des valeurs de perméabilité apparente (Papp) comprises entre 6,74 × 10⁻⁶ et 17,45 × 10⁻⁶ cm/s (Boerngen 2026). Cette caractéristique classe la molécule dans le Système de Classification Biopharmaceutique (BCS) de classe II ou IV selon les conditions expérimentales. L’ilunocitinib est un substrat des transporteurs d’efflux gastro-intestinaux, avec une homologie fonctionnelle avec la glycoprotéine-P (P-gp), propriété partagée avec le baricitinib et le tofacitinib en médecine humaine (Spinelli 2021).
2.2 Formulation galénique
2.2.1 Comprimés pelliculés et dosages
Les comprimés pelliculés de Zenrelia sont disponibles en quatre dosages : 4,8 mg, 6,4 mg, 8,5 mg et 15 mg d’ilunocitinib. Chaque comprimé est sécable, permettant une combinaison de plusieurs comprimés pour ajuster la dose au poids corporel de l’animal. Les comprimés d’ilunocitinib sont conditionnés en blisters de 10 et 30 unités et en flacons de 90 unités. La formulation hypoallergénique, non aromatisée, permet l’administration avec ou sans nourriture, sans effet significatif sur l’efficacité en conditions cliniques réelles (Boerngen 2026).
PARTIE III — MODE D’ACTION ET PHARMACODYNAMIE
3.1 La voie JAK-STAT : rappel fondamental
3.1.1 Architecture de la cascade de signalisation
La voie de signalisation JAK-STAT (Janus Kinase – Signal Transducer and Activator of Transcription) constitue l’un des mécanismes de transduction du signal cytokinique les plus conservés au cours de l’évolution des métazoaires. Cette voie assure la transmission du signal depuis les récepteurs cytokiniques membranaires de type I et II jusqu’au noyau cellulaire, où elle régule la transcription de gènes impliqués dans l’immunité, l’inflammation, l’hématopoïèse et la prolifération cellulaire (O’Shea 2015). La famille des kinases JAK comprend quatre membres : JAK1, JAK2, JAK3 et TYK2 (tyrosine kinase 2). Chaque kinase JAK est constituée de sept domaines d’homologie (JH1 à JH7), le domaine JH1 portant l’activité catalytique tyrosine-kinase et le domaine JH2 exerçant une fonction pseudokinase régulatrice. La famille des facteurs de transcription STAT comprend sept membres (STAT1 à STAT4, STAT5a, STAT5b, STAT6).
Le mécanisme de transduction suit une séquence ordonnée : la liaison de la cytokine à son récepteur membranaire induit la dimérisation du récepteur, entraînant le rapprochement et la trans-phosphorylation des kinases JAK associées à la portion intracytoplasmique du récepteur. Les JAK activées phosphorylent alors les résidus tyrosine du récepteur, créant des sites d’ancrage pour les protéines STAT. Les STAT recrutées sont à leur tour phosphorylées par les JAK, se dimérisent et transloquent vers le noyau où elles se lient aux éléments de réponse spécifiques sur l’ADN génomique, activant ou réprimant la transcription de gènes cibles (Spinelli 2021). L’inhibition pharmacologique de cette cascade par les inhibiteurs de JAK (JAKi) bloque simultanément la signalisation de multiples cytokines partageant les mêmes paires JAK, ce qui explique à la fois l’efficacité thérapeutique et le profil d’effets indésirables de cette classe médicamenteuse.
3.2 Sélectivité de l’ilunocitinib pour les sous-types JAK
3.2.1 Profil de sélectivité isoforme
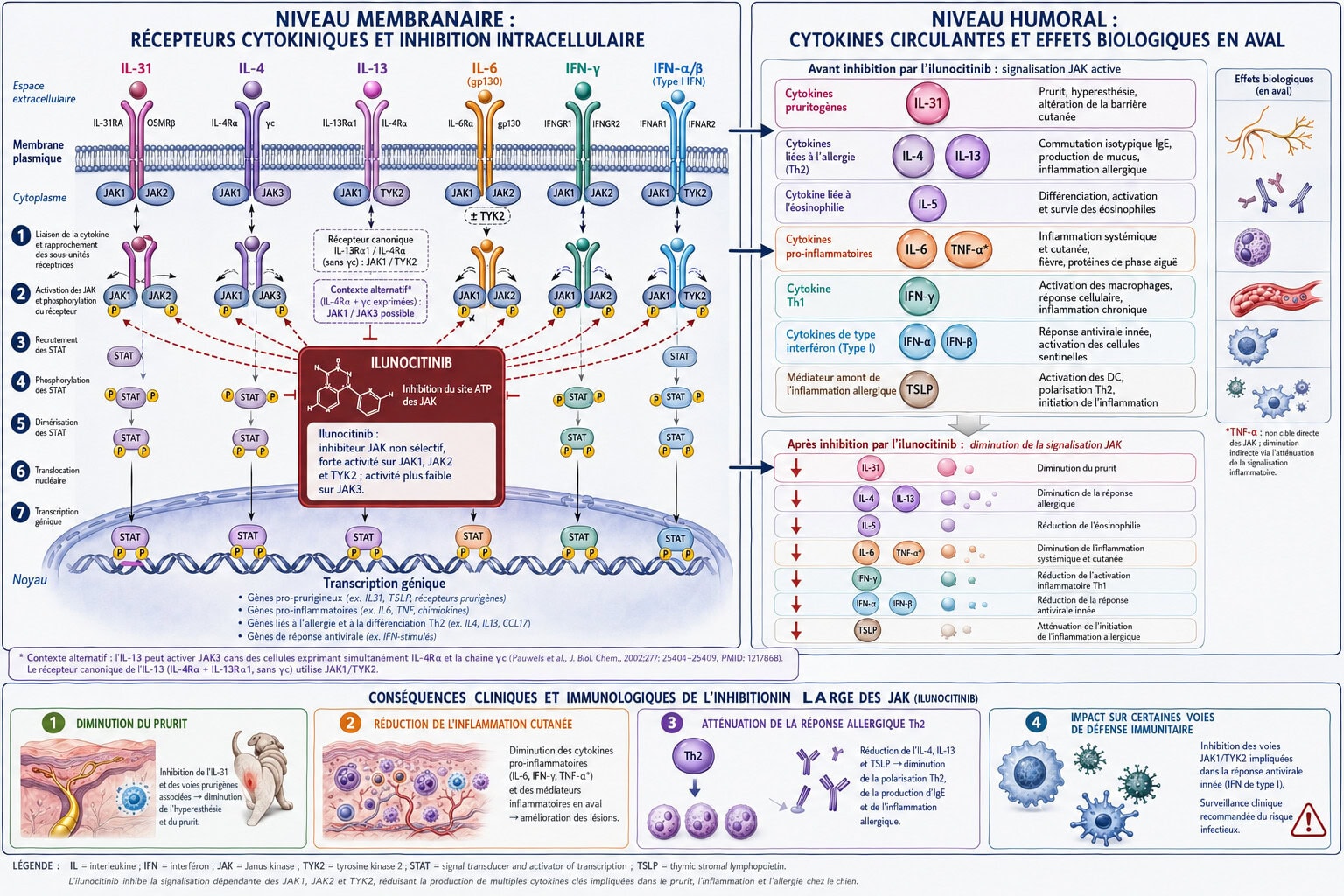
L’ilunocitinib est qualifié d’inhibiteur de JAK « non sélectif », avec un profil de sélectivité caractérisé par une haute puissance d’inhibition in vitro de JAK1, JAK2 et TYK2, et une activité moindre sur JAK3 (Forster 2025c). Cette sélectivité le distingue de l’oclacitinib, qui agit préférentiellement sur JAK1 et JAK3 (Gonzales 2014). L’inhibition de JAK1 est le mécanisme partagé par les deux molécules, responsable du blocage de la signalisation de l’IL-4 (via le complexe JAK1/JAK3), de l’IL-13 (via JAK1/TYK2 ou JAK1/JAK2) et de l’IL-31 (via JAK1/JAK2). L’inhibition de JAK2 par l’ilunocitinib implique un impact potentiel sur la voie de l’érythropoïétine (EPO/JAK2/STAT5), expliquant les modifications hématologiques dose-dépendantes observées dans l’étude de sécurité (Kuntz 2025). L’inhibition de TYK2 bloque la signalisation de l’IL-12 et de l’IL-23 (voie TYK2/JAK2-STAT4), impliquées dans la polarisation Th1/Th17, ajoutant une dimension anti-inflammatoire complémentaire. L’impact minimal sur les autres protéines kinases et lipide-kinases limite le risque d’effets hors cible (Choy 2019, Bonelli 2024). Toutefois, les données in vitro de sélectivité enzymatique ne prédisent pas directement l’efficacité et la tolérance clinique de la dermatite atopique traitée par JAKi, comme l’ont rappelé Virtanen et al. (Virtanen 2023) dans leur analyse comparative des profils de sélectivité isoforme des JAKi utilisés en rhumatologie humaine. Les essais cliniques comparatifs face à face restent le standard de référence pour la comparaison entre molécules.
3.3 Cytokines ciblées
3.3.1 Spectre d’inhibition cytokinique
L’inhibition des kinases JAK1, JAK2 et TYK2 par l’ilunocitinib bloque la signalisation d’un large spectre de cytokines impliquées dans la pathogénie de la DAC. Parmi les cytokines pruritogènes directement inhibées figurent l’IL-31 (médiateur majeur du prurit atopique canin, agissant via le complexe récepteur IL-31RA/OSMR et la paire JAK1/JAK2), la TSLP (thymic stromal lymphopoietin, cytokine d’alarme épithéliale activant la voie JAK1/JAK2-STAT5) et, indirectement, la substance P dont l’expression neuronale est modulée par les signaux IL-31-dépendants (Datsi 2021). Sur le plan neuroanatomique, le complexe récepteur IL-31RA/OSMR exprimé sur les neurones sensitifs cutanés transmet le signal pruritogène de l’IL-31 vers les ganglions de la racine dorsale (dorsal root ganglia), où s’opère le relais vers les voies ascendantes spinothalamiques aboutissant à la perception centrale du prurit (Nemmer 2021). Cette précision anatomique explique la rapidité d’action des JAKi sur le prurit : l’inhibition de la phosphorylation JAK1/JAK2 au niveau du neurone sensitif périphérique interrompt la cascade de signalisation en amont du premier relais synaptique.
Les cytokines pro-inflammatoires dont la signalisation est inhibée comprennent l’IL-4 (JAK1/JAK3 et JAK1/JAK2), l’IL-5 (JAK2-STAT3/5, impliquée dans l’éosinophilie), l’IL-13 (JAK1/JAK2/TYK2-STAT6, médiatrice de l’hyperplasie des cellules caliciformes et de la production d’IgE) et l’IFN-γ (JAK1/JAK2-STAT1). L’IL-33, cytokine d’alarme libérée par les kératinocytes lésés, signale principalement via le complexe ST2/IL-1RAcP et la voie MyD88/IRAK/NF-κB, activant les mastocytes résidents cutanés (Di Salvo 2018). Bien que certaines données expérimentales aient suggéré une phosphorylation de JAK2/STAT5 dans des modèles mastocytaires, la signalisation IL-33 n’est pas considérée comme JAK-dépendante au sens canonique, et l’impact de l’inhibition JAK sur l’activation mastocytaire induite par l’IL-33 reste à démontrer.
L’inhibition prononcée de JAK2 par l’ilunocitinib entrave la signalisation du facteur de stimulation des colonies de granulocytes-macrophages (GM-CSF), cytokine JAK2-dépendante impliquée dans la maturation, la survie et l’activation des cellules dendritiques et des macrophages tissulaires (Huang 2022). Cette inhibition de l’axe GM-CSF/JAK2 contribue à l’efficacité anti-inflammatoire de la molécule mais justifie une surveillance de la lignée myéloïde lors de traitements prolongés. Par ailleurs, l’impact de l’ilunocitinib sur TYK2 bloque la signalisation médiée par les interférons de type I (IFN-α/IFN-β), et non seulement celle de l’IFN-γ (type II). Les interférons de type I, signalant via la paire TYK2/JAK1-STAT1/STAT2, constituent la première ligne de défense antivirale innée. Dès lors, l’inhibition de cette voie par l’ilunocitinib explique mécanistiquement l’augmentation de la susceptibilité aux infections virales (adénovirose canine) observée en pharmacovigilance, au-delà de la seule immunosuppression adaptative (Spinelli 2021).
L’inhibition modérée de JAK3 par l’ilunocitinib (IC₅₀ = 16 nM, nettement inférieure à la puissance d’inhibition de JAK1 et JAK2) préserve partiellement l’immunité adaptative dépendante de la chaîne gamma commune (γc). La chaîne γc est le composant partagé des récepteurs de l’IL-2, de l’IL-7, de l’IL-15 et de l’IL-21, cytokines critiques pour la prolifération et la survie des cellules Natural Killer (NK) et des lymphocytes T de mémoire (Bonelli 2024). Cette préservation partielle de la signalisation JAK3/γc distingue l’ilunocitinib du tofacitinib humain (puissant inhibiteur de JAK3) et contribue au maintien de l’immunosurveillance antitumorale et antivirale à la dose thérapeutique. L’inhibition collatérale de l’IL-12, des interférons de type I et de l’IFN-γ, si elle produit un blanchiment lésionnel profond, génère une immunosuppression relative inhérente au mécanisme d’action vis-à-vis des cytokines de défense de l’hôte, qui doit être mise en balance avec le bénéfice clinique (Huang 2022). Le blocage de la voie IL-4/IL-13/STAT6 pourrait théoriquement contribuer à la réduction de la production d’IgE totales et spécifiques par les lymphocytes B, bien que cette hypothèse n’ait pas encore fait l’objet d’une démonstration formelle dans les études cliniques vétérinaires publiées à ce jour.
3.4 Comparaison pharmacodynamique avec les autres JAKi vétérinaires
3.4.1 Positionnement comparatif
L’ilunocitinib (Zenrelia), l’oclacitinib (Apoquel) et l’atinvicitinib représentent trois inhibiteurs de JAK aux profils pharmacodynamiques distincts. L’ilunocitinib inhibe principalement JAK1, JAK2 et TYK2 ; l’oclacitinib cible préférentiellement JAK1 et JAK2 (mais un faible impact fonctionnel sur les voies JAK2-dépendantes (érythropoïétine)) et l’atinvicitinib est un inhibiteur sélectif de JAK1 de seconde génération (Bonelli 2024). Sur le plan posologique, l’ilunocitinib présente l’avantage d’une administration quotidienne unique sans dose de charge, contre une administration biquotidienne pendant 14 jours puis quotidienne pour l’oclacitinib. Cette différence posologique supprime le risque de rebond du prurit lors du passage à la dose d’entretien, phénomène documenté avec l’oclacitinib (Olivry 2023, Fukuyama 2017). L’inhibition de JAK2 par l’ilunocitinib, absente du profil de l’oclacitinib, pourrait expliquer les modifications hématologiques observées à forte dose mais confère un spectre anti-inflammatoire plus large couvrant la voie IFN-γ (Bonelli 2024).
PARTIE IV — PHARMACOCINÉTIQUE
4.1 Absorption
4.1.1 Biodisponibilité et effet prandial
Après administration orale, l’ilunocitinib est rapidement absorbé, avec un temps médian pour atteindre la concentration plasmatique maximale (Tmax) compris entre 1 et 4 heures selon l’état de jeûne (Boerngen 2026). L’effet de l’alimentation sur la biodisponibilité a été caractérisé de manière détaillée. La biodisponibilité absolue est de 79,6 % (IC 90 % : 67,6-93,6 %) avec un repas contre 60,8 % (IC 90 % : 51,6-71,5 %) à jeun. Les concentrations maximales moyennes (Cmax) à la dose de 0,8 mg/kg sont de 268 ng/mL (avec un repas) contre 122 ng/mL (à jeun). Malgré cet effet prandial significatif en conditions de laboratoire sur dose unique, l’absence de différence pharmacocinétique cliniquement significative a été confirmée dans les trois études de terrain, où les propriétaires administraient le médicament vétérinaire avec ou sans repas selon leur convenance (Forster 2025a, 2025b, 2025c). Cette discordance entre les données de laboratoire et les données de terrain est attribuée à l’atténuation de l’effet prandial en conditions d’administration répétée.
4.2 Distribution
4.2.1 Paramètres de distribution
Après administration intraveineuse, l’ilunocitinib présente une clairance plasmatique de 0,437 L/h/kg (7,3 mL/min/kg) et un volume de distribution à l’équilibre (Vss) de 1,58 L/kg (Boerngen 2026). Un Vss supérieur à 1 L/kg indique une distribution tissulaire large, dépassant le compartiment plasmatique et le volume d’eau corporelle totale. Les études de distribution tissulaire ont révélé une forte accumulation dans la bile, le foie et les reins, organes impliqués dans le métabolisme et l’élimination de la molécule. La pénétration à travers la barrière hémato-encéphalique est faible, ce qui est cohérent avec l’absence d’effets neurologiques observés dans l’étude de sécurité sur 6 mois (Kuntz 2025).
4.3 Métabolisme et élimination
4.3.1 Voies d’élimination et demi-vie
L’élimination de l’ilunocitinib emprunte une double voie : environ 50 % de la dose administrée est éliminée par voie biliaire et fécale, et environ 30 % par voie urinaire, soit un taux de récupération d’environ 80 % à 48 heures (Boerngen 2026). La demi-vie d’élimination terminale est de 4,4 heures après administration intraveineuse et d’environ 5 heures après administration orale. Cette demi-vie relativement courte est compatible avec une administration quotidienne unique et explique l’absence d’accumulation cliniquement significative observée lors de l’administration répétée : le rapport d’accumulation moyen sur l’AUC (aire sous la courbe) en administration à doses multiples est d’environ 1,26 (Boerngen 2026). L’étude de sécurité sur 6 mois a confirmé des rapports d’accumulation AUC de 1,2 à 1,6 selon les groupes de dose, sans différence entre mâles et femelles (Kuntz 2025).
4.4 Proportionnalité à la dose
4.4.1 Linéarité de l’exposition
L’augmentation de l’exposition systémique (AUC et Cmax) est linéaire mais non proportionnelle à la dose sur l’intervalle posologique de 0,4 à 4,0 mg/kg, avec un intercept statistiquement significatif dans l’analyse de régression (Boerngen 2026). Ce phénomène est attribué à une absorption limitée par la solubilité à forte concentration intraluminale, compatible avec les propriétés physicochimiques de la molécule (faible solubilité aqueuse). Cette non-proportionnalité a été confirmée dans l’étude de sécurité à doses multiples (Kuntz 2025), où l’exposition à la dose de 4,0 mg/kg (5X) était inférieure à cinq fois l’exposition à la dose thérapeutique.
4.5 Pharmacocinétique en conditions cliniques réelles
4.5.1 Données de terrain
Les données pharmacocinétiques recueillies dans les trois essais cliniques de terrain (études placebo-contrôlées et étude comparative avec l’oclacitinib) confirment l’absence de différence cliniquement significative liée à l’état alimentaire en conditions d’utilisation réelle (Forster 2025a, 2025b, 2025c). L’efficacité constante observée indépendamment de l’administration avec ou sans nourriture constitue un avantage pratique pour l’observance thérapeutique par les propriétaires, en particulier lors de traitements prolongés chez le chien atopique.
PARTIE V — INDICATIONS ET POSOLOGIE
5.1 Indications autorisées
5.1.1 Cadre de l’AMM
Le Zenrelia (comprimés d’ilunocitinib) est indiqué pour le contrôle du prurit associé aux dermatites allergiques et le contrôle de la dermatite atopique chez le chien âgé d’au moins 12 mois. L’indication couvre le prurit associé aux dermatites allergiques au sens large, incluant la dermatite atopique (sensibilisation aux aéroallergènes), la dermatite par allergie aux piqûres de puces (DAPP) et l’hypersensibilité alimentaire à composante prurigineuse, ce qui en fait un traitement polyvalent des dermatites allergiques canines. La distinction entre DAC et dermatites allergiques a été documentée par des essais cliniques distincts (Forster 2025a pour la dermatite allergique, Forster 2025b pour la DAC).
5.2 Posologie et mode d’administration
5.2.1 Schéma posologique
La dose thérapeutique recommandée est de 0,6 à 0,8 mg/kg d’ilunocitinib en une administration orale unique quotidienne, avec ou sans nourriture. Le calcul de la dose individuelle s’effectue par combinaison des quatre dosages de comprimés disponibles (4,8 ; 6,4 ; 8,5 ; 15 mg) en fonction du poids de l’animal. Aucune dose de charge n’est requise : le traitement débute directement à la dose quotidienne définitive, ce qui simplifie le schéma posologique par rapport à l’oclacitinib. Aucune durée maximale de traitement n’est spécifiée dans le RCP, compte tenu de l’absence d’accumulation cliniquement significative et de la tolérance documentée sur 112 jours dans les essais cliniques et 182 jours dans l’étude de sécurité.
5.3 Début et durée d’action
5.3.1 Cinétique de la réponse thérapeutique
L’efficacité anti-prurigineuse de l’ilunocitinib est détectable dès les premières 24 heures et devient statistiquement significative dès J3 : dans l’étude sur la dermatite allergique, 29 % des chiens traités présentaient une réduction du prurit supérieure ou égale à 50 % (PVAS) dès le troisième jour de traitement (Forster 2025a). À J7, le taux de succès thérapeutique (réduction ≥ 50 % du PVAS) était de 25,4 % dans le groupe ilunocitinib contre 7,7 % dans le groupe placebo (p = 0,006). L’efficacité sur les lésions cutanées, évaluée par le score CADESI-04 (Olivry 2014), devient significative dès J14. À J28, 83 % des chiens traités atteignaient le critère de succès thérapeutique contre 31 % sous placebo (p < 0,001) dans l’étude pivot européenne sur la DAC (Forster 2025b). La rémission clinique, définie par un score PVAS inférieur à 2 (correspondant à un niveau de prurit « normal ») ou un score CADESI-04 inférieur à 10, était atteinte chez les deux tiers des chiens après 4 mois de traitement (Forster 2025b).
PARTIE VI — ÉTUDES CLINIQUES D’EFFICACITÉ
6.1 Étude pivot placebo-contrôlée (Europe/USA)
6.1.1 Protocole et résultats
L’essai pivot publié par Forster, Trout, Despa et al. dans Veterinary Dermatology (2025) a évalué l’efficacité et la sécurité de l’ilunocitinib dans le contrôle de la dermatite atopique canine. Le protocole était un essai randomisé, en double aveugle, contrôlé par placebo, mené dans 25 cliniques vétérinaires en Grande-Bretagne et en Allemagne. Deux cent soixante-huit chiens atteints de DAC confirmée ont été inclus : 181 dans le groupe ilunocitinib (0,6-0,8 mg/kg/jour) et 87 dans le groupe placebo, pour une durée de 112 jours (Forster 2025b). Les races les plus représentées étaient le Labrador Retriever, le Bouledogue Français, le West Highland White Terrier et le Golden Retriever (5,6 %). L’âge des chiens inclus variait de 1,0 à 17,3 ans.
Le critère d’évaluation principal était le taux de succès thérapeutique à J28, défini par une réduction supérieure ou égale à 50 % du score PVAS (prurit évalué par le propriétaire) ou du score CADESI-04 (lésions cutanées évaluées par l’investigateur). Les résultats ont démontré une supériorité statistiquement significative de l’ilunocitinib sur le placebo à tous les temps d’évaluation. À J28, 83 % des chiens du groupe ilunocitinib atteignaient le critère de succès sur le PVAS contre 31 % dans le groupe placebo (p < 0,001) (Forster 2025b). La proportion de chiens atteignant la rémission clinique du prurit (PVAS < 2) était significativement plus élevée dans le groupe ilunocitinib dès J7 (p < 0,05), et la rémission des lésions cutanées (CADESI-04 < 10) dès J14 (p < 0,05). Aucun chien du groupe placebo n’avait atteint le seuil CADESI-04 < 10 à J28. La proportion cumulative de chiens sortis de l’étude pour inefficacité perçue était significativement plus élevée dans le groupe placebo. Le traitement de 112 jours a été bien toléré.
6.2 Étude comparative ilunocitinib vs oclacitinib
6.2.1 Résultats comparatifs
L’essai comparatif publié par Forster, Boegel, Despa et al. dans Veterinary Dermatology (2025) a évalué l’efficacité et la sécurité de l’ilunocitinib en comparaison directe avec l’oclacitinib chez des chiens atteints de DAC. L’essai était randomisé, en aveugle, mené dans 25 centres dans quatre pays européens. Trois cent trente-huit chiens ont été randomisés pour recevoir soit l’oclacitinib (0,4-0,6 mg/kg deux fois par jour pendant 14 jours, puis une fois par jour) soit l’ilunocitinib (0,6-0,8 mg/kg une fois par jour), pour une durée maximale de 112 jours (Forster 2025c). La réduction du prurit (PVAS) et des scores CADESI-04 était comparable entre les deux groupes pendant les 14 premiers jours de traitement (J0-J14), période correspondant à la phase biquotidienne de l’oclacitinib. Par contre, entre J14 et J28, les scores PVAS augmentaient dans le groupe oclacitinib (phénomène de rebond lors du passage à la dose d’entretien) tandis qu’ils continuaient à diminuer dans le groupe ilunocitinib. De J28 à J112, les scores PVAS et CADESI-04 moyens étaient significativement plus faibles dans le groupe ilunocitinib (p ≤ 0,003 et p ≤ 0,023, respectivement). Un nombre significativement plus élevé de chiens traités par ilunocitinib atteignait la rémission clinique du prurit (PVAS < 2) de J28 à J112. L’évaluation subjective globale de la réponse thérapeutique par les investigateurs était significativement meilleure pour l’ilunocitinib de J28 à J112 (p ≤ 0,002). Les profils de tolérance étaient comparables entre les deux groupes (Forster 2025c).
6.3 Études sur la dermatite allergique (non atopique)
6.3.1 Essai USA placebo-contrôlé
L’essai randomisé, en double aveugle, contrôlé par placebo, publié par Forster, Trout, Despa et al. dans Veterinary Dermatology (2025) a évalué l’ilunocitinib chez 306 chiens présentant un prurit sévère et un diagnostic présomptif de dermatite allergique, recrutés dans 15 cliniques vétérinaires aux États-Unis (Forster 2025a). Les chiens ont été randomisés pour recevoir l’ilunocitinib (n = 206 ; 0,6-0,8 mg/kg) ou le placebo (n = 100) une fois par jour pendant 28 jours, avec un suivi de sécurité sur 112 jours. Plus de 90 % des chiens dans chaque groupe avaient un diagnostic présomptif de DAC, avec des diagnostics concomitants incluant la dermatite de contact (23,3 %), la DAPP (15,5 %) et l’hypersensibilité alimentaire (24,3 %). Le critère principal était le taux de succès thérapeutique à J7, défini par une réduction ≥ 50 % du PVAS pendant au moins 5 des 7 premiers jours. À J7, 25,4 % des chiens traités par ilunocitinib atteignaient ce critère contre 7,7 % sous placebo (p = 0,006). Dès J3, la proportion de chiens présentant une réduction ≥ 50 % du PVAS était significativement plus élevée dans le groupe ilunocitinib (p < 0,01). À J28, 51,8 % des chiens traités atteignaient la rémission clinique (PVAS < 2) contre 12,7 % sous placebo (p < 0,05). Les manifestations de dermatite s’amélioraient dès J7. Le traitement de 112 jours était bien toléré (Forster 2025a).
PARTIE VII — DONNÉES DE SÉCURITÉ
7.1 Étude de sécurité sur espèce cible (6 mois)
7.1.1 Protocole
L’étude de sécurité publiée par Kuntz, Gabor et Toutain dans BMC Veterinary Research (2025) constitue la pierre angulaire du dossier de sécurité de l’ilunocitinib. Le protocole, conduit conformément aux recommandations VICH GL43, était un essai randomisé, en aveugle, en groupes parallèles, incluant 40 Beagles sains (20 mâles et 20 femelles), âgés de 11 à 12 mois, avec un poids moyen de 9,85 à 10,46 kg (Kuntz 2025). Les animaux ont été répartis en un groupe témoin non traité et quatre groupes recevant l’ilunocitinib à des doses quotidiennes de 0,8 mg/kg (1X, dose thérapeutique maximale recommandée), 1,6 mg/kg (2X), 2,4 mg/kg (3X) et 4,0 mg/kg (5X) pendant 182 jours. Tous les animaux étaient nourris dans les 30 minutes précédant l’administration. Les évaluations de sécurité comprenaient les observations cliniques générales, les examens physiques et neurologiques complets (toutes les deux semaines), les examens ophtalmologiques, l’hématologie, la biochimie sérique, la coagulation, l’immunophénotypage des lymphocytes périphériques, le poids corporel, la consommation alimentaire, les prélèvements pharmacocinétiques et les examens macroscopiques et histopathologiques des organes en fin d’étude.
7.1.2 Résultats
À la dose thérapeutique (1X = 0,8 mg/kg), aucun effet indésirable cliniquement significatif n’a été rapporté. Aucun effet du traitement n’a été observé sur le poids corporel, la consommation alimentaire, les examens physiques et neurologiques, l’analyse urinaire, l’immunophénotype des lymphocytes périphériques (CD5+ T totaux, CD4+ Th, CD8+ Tc, CD21+ B, monocytes) ni les examens ophtalmologiques (Kuntz 2025). Aux doses supérieures, des lésions cutanées interdigitées (furonculose, kystes folliculaires interdigités) sont apparues de manière dose-dépendante, plus fréquentes aux doses ≥ 3X, évoluant vers la résolution spontanée ou après traitement antimicrobien standard. Une légère diminution des paramètres érythrocytaires (hémoglobine, hématocrite, numération des globules rouges, CCMH, TCMH) a été observée aux doses ≥ 3X, les valeurs restant dans les limites de référence au palier 1X. Une diminution des éosinophiles a été notée chez les femelles aux doses ≥ 3X (p = 0,0050). Une augmentation du fibrinogène et de la protéine C réactive aux doses ≥ 3X (p < 0,0001 pour le fibrinogène) a été interprétée comme une réponse de phase aiguë secondaire aux lésions cutanées interdigitées. Des papillomes cutanés ont été observés chez 2 chiens à la dose 5X, avec résolution spontanée attendue. Une légère modification des poids surrénaliens a été notée sans corrélation histopathologique. Aucun effet hépatique, rénal, oculaire ou neurologique n’a été documenté. Aucune mortalité ni aucun effet indésirable grave n’est survenu pendant les 182 jours d’étude, y compris à 5X la dose maximale recommandée, et tous les animaux traités ont achevé la durée prévue de l’étude (Kuntz 2025).
7.2 Sécurité dans les essais cliniques de terrain
7.2.1 Compilation des données de tolérance
Les données de tolérance compilées à partir des trois essais cliniques (Forster 2025a, 2025b, 2025c) portent sur plus de 500 chiens traités par ilunocitinib en conditions réelles. Les effets indésirables les plus fréquemment rapportés étaient des troubles digestifs et de la léthargie. Les données du dossier d’enregistrement FDA précisent les incidences spécifiques dans les essais de terrain : diarrhées chez 12,2 % et infections du tractus urinaire chez 6,3 % (FDA 2024). L’incidence globale des effets indésirables gastro-intestinaux dans l’étude sur la dermatite allergique (Forster 2025a) était comparable entre le groupe traité et le groupe placebo à J28 : 47,6 % contre 49,0 %, démontrant que l’ilunocitinib n’augmente pas l’incidence des troubles digestifs par rapport au placebo. Des conditions néoplasiques (bénignes et malignes) ont été observées pendant les études cliniques, motivant la recommandation de surveillance chez les chiens présentant un antécédent de néoplasie récurrente. L’étude pivot sur la DAC a rapporté une légère augmentation de l’albumine dans le groupe ilunocitinib aux temps J56, J84 et J112, sans signification clinique déterminée (Forster 2025b). Un cas isolé de neutropénie cyclique a été identifié chez un chien traité, considéré comme non lié au traitement. La numération des plaquettes est restée dans les limites de référence dans l’ensemble des études (Forster 2025b, Kuntz 2025). Dans l’étude comparative avec l’oclacitinib, les taux d’événements indésirables étaient similaires entre les deux groupes, confirmant un profil de tolérance comparable (Forster 2025c).
7.3 Données post-marketing
7.3.1 Pharmacovigilance internationale
Depuis le lancement commercial au Brésil (premier marché), puis aux États-Unis, au Japon, au Canada et en Europe, plus de 800 000 chiens ont été traités par Zenrelia à la date de septembre 2025, selon les données communiquées par Elanco. La pharmacovigilance post-AMM a conduit à l’identification de signaux concernant la susceptibilité aux infections (hépatite adénovirale, pancréatite) et un risque d’inadéquation de la réponse immunitaire vaccinale, intégrés dans les mises en garde du RCP. En septembre 2025, l’analyse PCR rétrospective des tissus hépatiques des deux chiens euthanasiés dans l’étude de réponse vaccinale initiale a révélé la présence de CAV-1 (adénovirus canin de type 1, agent de l’hépatite infectieuse canine par infection naturelle), suggérant qu’une épizootie naturelle, et non une maladie vaccinale induite, était à l’origine de la détérioration clinique de ces animaux (Fent 2025a). La FDA a conclu que la totalité des preuves soutenait le retrait du risque de maladie vaccinale fatale induite par les vaccins à virus vivants modifiés de l’étiquetage.
PARTIE VIII — CONTRE-INDICATIONS ET PRÉCAUTIONS D’EMPLOI
8.1 Contre-indications absolues
8.1.1 Situations d’exclusion
L’ilunocitinib ne doit pas être utilisé chez les chiens de moins de 12 mois, chez les chiens présentant une infection grave, ni chez les chiens atteints d’une néoplasie maligne avérée, d’une démodécie ou d’un état d’immunosuppression (hyperadrénocorticisme, par exemple), situations dans lesquelles la molécule n’a pas été évaluée. L’absence de données sur les chiens reproducteurs, les femelles gestantes ou allaitantes constitue une contre-indication relative. L’accès au traitement est donc réservé aux chiens adultes, en bonne santé générale, à jour de leur vaccination.
8.2 Mise en garde vaccination
8.2.1 Études de réponse vaccinale
L’effet de l’administration d’ilunocitinib sur la vaccination contre le parvovirus canin (CPV), le virus de la maladie de Carré (CDV), l’adénovirus canin-2 (CAV-2), le parainfluenza canin (CPiV) et le vaccin inactivé contre la rage (RV) a été étudié dans deux protocoles distincts. L’étude de primo-vaccination (Fent 2025a) a été conduite chez des Beagles de 10 mois, séronégatifs, naïfs de vaccination, recevant 2,4 mg/kg (3X la dose maximale recommandée) pendant 89 jours. Au cours de cette étude, une épizootie de coccidiose (Cystoisospora canis) et un cas confirmé d’hépatite infectieuse canine (CAV-1) sont survenus, confondant l’interprétation des résultats. Deux chiens traités ont été euthanasiés en raison de la dégradation de leur état général. Sur la base de l’évaluation des titres d’anticorps sérologiques, une réponse immunitaire adéquate aux vaccins vivants atténués canins courants (CAV-2, CDV et CPV) a été observée après la primo-vaccination au jour 28. La réponse à la primo-vaccination par le CPiV (vaccin non essentiel) chez les animaux traités était de 4 sur 6 au-dessus du seuil contre 6 sur 8 au-dessus du seuil pour les animaux témoins. Une réponse retardée ou réduite au RV a été observée (Fent 2025a).
L’étude de rappel vaccinal (Fent 2025b), publiée dans BMC Veterinary Research, a évalué la réponse sérologique au rappel de vaccination chez des chiens de 10 mois préalablement vaccinés selon les recommandations standard, recevant l’ilunocitinib à 1X ou 3X la dose recommandée (0,6-0,8 ou 1,8-2,4 mg/kg, respectivement) pendant 56 jours. Les résultats ont démontré que le traitement par ilunocitinib aux doses 1X et 3X n’atténuait pas significativement la réponse sérologique aux rappels vaccinaux CAV-2, CPV, CDV ou rage par rapport aux animaux témoins non traités (Fent 2025b). Tous les chiens traités présentaient des titres d’anticorps à un niveau supérieur ou égal au seuil protecteur pour la rage, le CAV-2 et le CPV aux jours 43 et 56 post-vaccination. Le RCP actuel maintient la recommandation d’interrompre le Zenrelia au moins 28 jours à 3 mois avant toute vaccination et de ne pas reprendre le traitement avant au moins 28 jours après la vaccination. Les chiens doivent être à jour de leur vaccination avant l’initiation du traitement.
La conclusion de la FDA est que la dose thérapeutique (0,6–0,8 mg/kg) ne présente pas de risque documenté de maladie vaccinale fatale induite, après révision du label en septembre 2025
8.3 Risques infectieux et surveillance
8.3.1 Susceptibilité infectieuse et protocole de suivi
L’immunomodulation induite par l’inhibition des kinases JAK entraîne une augmentation théorique de la susceptibilité aux infections opportunistes. Les infections documentées dans les études cliniques de la dermatite atopique et dans la pharmacovigilance post-AMM comprennent les infections bactériennes cutanées (pyodermites), les infections des voies respiratoires, les infections urinaires, la réactivation de Demodex canis et les infections parasitaires intestinales (coccidiose). L’adénovirose canine (hépatite et pancréatite) a été identifiée comme signal de pharmacovigilance. Un protocole de surveillance clinique est recommandé, incluant un examen physique régulier, un hémogramme de contrôle (recherche d’anomalies des paramètres érythrocytaires : hémoglobine, hématocrite, numération des plaquettes et des globules rouges) et une vigilance accrue vis-à-vis des infections cutanées, respiratoires et digestives (Kuntz 2025).
8.4 Risque néoplasique
8.4.1 Balance bénéfice/risque
Des conditions néoplasiques bénignes et malignes ont été observées au cours des études cliniques de l’ilunocitinib, sans qu’un lien de causalité ait été formellement établi (Forster 2025b). Par analogie avec les données accumulées en médecine humaine sur les JAKi (tofacitinib, baricitinib, upadacitinib), une surveillance de l’émergence de néoplasies lors d’utilisation prolongée est recommandée, en particulier chez les chiens présentant un antécédent de néoplasie récurrente. La balance bénéfice/risque doit être évaluée individuellement pour chaque patient.
8.5 Populations à risque particulier
8.5.1 Populations non évaluées
Les chiens âgés, les races présentant une susceptibilité infectieuse particulière (races brachycéphales, races à prédisposition démodécique) et les chiens sous traitement immunosuppresseur concomitant constituent des populations à risque accru nécessitant une surveillance renforcée. L’absence de données chez les chiots de moins de 12 mois, les femelles gestantes ou allaitantes et les chiens reproducteurs impose une extrapolation prudente. L’association avec d’autres immunosuppresseurs (glucocorticoïdes, ciclosporine) n’a pas été évaluée dans le cadre du programme de développement clinique (Kuntz 2025).
PARTIE IX — INTERACTIONS MÉDICAMENTEUSES
9.1 Interactions pharmacodynamiques
L’association de l’ilunocitinib avec d’autres agents immunosuppresseurs (glucocorticoïdes systémiques, ciclosporine, azathioprine, mycophénolate mofétil) est susceptible de potentialiser l’immunosuppression et d’accroître le risque infectieux (EMA 2025). Cette association n’est pas recommandée sans une évaluation rigoureuse de la balance bénéfice/risque au cas par cas. Les données des essais cliniques ont été recueillies dans des conditions où les traitements anti-infectieux (antibiotiques, antifongiques, antiparasitaires) et les topiques non stéroïdiens étaient autorisés en concomitance, et les vaccinations étaient permises selon le protocole de l’étude (Forster 2025a, 2025b, 2025c). L’association ilunocitinib et immunothérapie allergénique spécifique (ASIT, désensibilisation) constitue une perspective clinique étayée par les données disponibles : Fennis et al. (2022) ont démontré dans un essai prospectif portant sur 48 chiens atopiques que l’administration concomitante d’oclacitinib et d’ASIT n’entravait pas la modulation lymphocytaire induite par l’immunothérapie, les taux de réponse clinique restant comparables à ceux des chiens recevant l’ASIT seule. Par extrapolation pharmacodynamique (mécanisme JAK partagé), le maintien de l’ilunocitinib pendant les phases d’induction de la désensibilisation apparaît compatible avec l’efficacité de l’ASIT, la désensibilisation agissant via l’induction de tolérance par les lymphocytes T régulateurs et les IgG bloquantes — mécanismes immunologiques distincts de la voie JAK-STAT (Fennis 2022).
9.2 Interactions pharmacocinétiques
9.2.1 Substrat de la P-glycoprotéine
L’ilunocitinib est un substrat potentiel des transporteurs P-gp (ABCB1) au niveau intestinal, par analogie avec le baricitinib et le tofacitinib (Spinelli 2021). Les médicaments inhibant la P-gp (kétoconazole, itraconazole, ciclosporine, vérapamil) pourraient théoriquement augmenter la biodisponibilité de l’ilunocitinib en réduisant l’efflux intestinal, tandis que les inducteurs de la P-gp (rifampicine, phénobarbital) pourraient la diminuer (Payne 2015). Leur co-administration avec l’ilunocitinib pourrait augmenter l’exposition systémique de ce dernier par compétition sur le transporteur d’efflux ABCB1.
9.2.2 Interactions avec les cytochromes P450 canins
L’influence des cytochromes P450 hépatiques sur le métabolisme de l’ilunocitinib n’a pas été entièrement caractérisée in vivo chez le chien, bien que les données de métabolisme suggèrent une contribution significative de la voie biliaire à l’élimination (Boerngen 2026). Le CYP2D15 canin, orthologue du CYP2D6 humain, métabolise de nombreux médicaments psychotropes et cardiovasculaires. La clomipramine (CLOMICALM cp 5-20-80 mg ND, Elanco), tricyclique fréquemment prescrit dans le traitement des troubles anxieux du chien atopique (anxiété de séparation, dermatite de léchage), est un inhibiteur documenté du CYP2D15 canin (Aidasani 2008). L’administration concomitante d’ilunocitinib et de clomipramine pourrait théoriquement modifier le profil métabolique de l’un ou l’autre composé si le CYP2D15 contribue significativement à leur biotransformation. La prudence est de mise lors de l’administration concomitante de médicaments substrats ou inhibiteurs des transporteurs d’efflux ou des CYP hépatiques (EMA 2025).
PARTIE X — DONNÉES IMMUNOLOGIQUES APPROFONDIES
10.1 Impact sur les sous-populations lymphocytaires
L’immunophénotypage des lymphocytes périphériques réalisé dans l’étude de sécurité sur 6 mois (Kuntz 2025) a démontré l’absence d’effet significatif de l’ilunocitinib sur les sous-populations lymphocytaires CD5+ T totaux, CD4+ T auxiliaires, CD8+ T cytotoxiques, CD21+ B et monocytes à la dose thérapeutique (0,8 mg/kg). Cette préservation de l’immunophénotype circulant à la dose clinique contraste avec les données humaines du tofacitinib, pour lequel une réduction dose-dépendante des lymphocytes NK (natural killer) et des lymphocytes T CD8+ a été documentée en rhumatologie humaine (Strober 2013). L’absence de perturbation des populations lymphocytaires à la dose thérapeutique constitue un argument de tolérance immunologique significatif, suggérant que le maintien de l’immunité adaptative est compatible avec l’efficacité anti-prurigineuse et anti-inflammatoire de la molécule. Toutefois, la surveillance hématologique régulière reste recommandée lors d’utilisation prolongée, les données de sécurité à très long terme (au-delà de 6 mois) n’étant pas encore disponibles dans des études contrôlées.
10.2 Impact sur l’érythropoïèse
Une diminution légère et dose-dépendante des paramètres érythrocytaires (hémoglobine, hématocrite, numération des globules rouges, CCMH, TCMH) a été documentée aux doses ≥ 3X dans l’étude de sécurité (Kuntz 2025). Ce phénomène est attribué à l’inhibition de la signalisation JAK2/EPO (érythropoïétine), voie critique de l’érythropoïèse médullaire. La liaison de l’EPO à son récepteur homodimérique active la paire JAK2/JAK2, induisant la phosphorylation de STAT5 et la transcription des gènes de survie et de prolifération des progéniteurs érythroïdes. L’inhibition de JAK2 par l’ilunocitinib entraîne une atténuation dose-dépendante de cette cascade, avec des conséquences cliniques restant infraliminaires à la dose thérapeutique (valeurs restant dans les limites de référence), mais pouvant devenir significatives en cas de surdosage prolongé. Cette observation est cohérente avec les données des JAKi humains : le baricitinib induit une diminution modérée de l’hémoglobine chez 2 à 5 % des patients humains traités pour polyarthrite rhumatoïde, et le tofacitinib a été associé à des cas d’anémie nécessitant une réduction posologique (Strober 2013). La surveillance de l’hémogramme, en particulier de l’hématocrite et de l’hémoglobine, est recommandée lors de l’utilisation à long terme de l’ilunocitinib, avec une avancée posologique prudente chez les chiens anémiés ou présentant une santé médullaire fragile.
10.3 Effet sur la voie Th2 et l’axe IL-4/IL-13 : Implications thérapeutiques au-delà du prurit
L’inhibition de la signalisation IL-4/IL-13 par le blocage des paires JAK1/JAK3 et JAK1/JAK2/TYK2 constitue l’un des mécanismes pharmacodynamiques centraux de l’ilunocitinib, avec des implications thérapeutiques potentiellement plus larges que le seul contrôle du prurit. L’IL-4, en se liant à son récepteur de type I (IL-4Rα/γc, JAK1/JAK3) ou de type II (IL-4Rα/IL-13Rα1, JAK1/TYK2), active la phosphorylation de STAT6, facteur de transcription clé de la polarisation Th2. STAT6 phosphorylé induit la transcription des gènes codant pour la chaîne ε des immunoglobulines (commutation isotypique vers l’IgE), les récepteurs aux chimiokines CCR4 et CCR8, et les médiateurs pro-inflammatoires Th2 (IL-5, IL-13) (Olivry 2010). L’inhibition de cette voie par l’ilunocitinib pourrait théoriquement réduire la production d’IgE totales et spécifiques, contribuer à la restauration de la barrière cutanée (l’IL-13 altérant l’expression des protéines de jonction kératinocytaires) et exercer un effet anti-inflammatoire dépassant le cadre du contrôle symptomatique du prurit et des démangeaisons. Ces hypothèses mécanistiques constituent des axes de recherche futurs, les données cliniques actuelles ne permettant pas de documenter une réduction des IgE sériques sous ilunocitinib dans les essais publiés. L’étude comparative avec l’oclacitinib (Forster 2025c) a mis en évidence une diminution plus marquée et plus soutenue des lésions cutanées (CADESI-04) sous ilunocitinib de J28 à J112, suggérant un effet anti-inflammatoire cutané allant au-delà du simple contrôle antiprurigineux et possiblement lié à l’inhibition complémentaire de TYK2 (voie IL-12/IL-23-Th1/Th17).
Perspectives de recherche
L’arrivée de l’ilunocitinib dans l’arsenal thérapeutique de la dermatologie vétérinaire ouvre plusieurs axes d’investigation. Les données de sécurité à très long terme (au-delà de 12 mois) en conditions cliniques réelles restent nécessaires, en particulier pour caractériser le risque néoplasique et infectieux cumulatif. En médecine humaine, l’étude ORAL Surveillance a mis en évidence un risque accru d’événements cardiovasculaires majeurs et de néoplasies sous tofacitinib par rapport aux anti-TNF chez les patients rhumatologiques de plus de 50 ans, conduisant la FDA à émettre un avertissement encadré pour l’ensemble des JAKi humains. L’extrapolation de ces données à la médecine vétérinaire reste spéculative, la physiopathologie cardiovasculaire canine et l’espérance de vie des patients étant fondamentalement différentes, mais la vigilance oncologique et infectieuse s’impose lors de traitements prolongés.
L’impact de l’ilunocitinib sur le microbiome cutané des chiens atopiques, sur la restauration de la barrière épidermique et sur les biomarqueurs sériques (IgE totales et spécifiques, cytokines circulantes) mérite une évaluation prospective. Les études transcriptomiques menées sur des biopsies cutanées de chiens atopiques traités par oclacitinib ont démontré une normalisation partielle de l’expression des protéines de jonction intercellulaire et des peptides antimicrobiens (Marsella 2021), suggérant que l’inhibition JAK pourrait exercer un effet de restauration barrière au-delà du seul contrôle symptomatique. Des études similaires avec l’ilunocitinib, tirant parti de son profil d’inhibition complémentaire (TYK2), permettraient de documenter un éventuel avantage thérapeutique sur la biologie de la barrière cutanée.
L’association ilunocitinib et immunothérapie allergénique spécifique (ASIT) pourrait constituer une stratégie combinée alliant le contrôle symptomatique rapide à la modification à long terme de la réponse immunitaire allergique. L’ASIT, dont l’efficacité est documentée chez 50 à 75 % des chiens atopiques, selon les études et les protocoles, après 6 à 12 mois de protocole (Olivry 2015), agit par induction de lymphocytes T régulateurs producteurs d’IL-10 et de TGF-β et par déviation isotypique des IgE vers les IgG4 bloquantes. Le maintien des populations lymphocytaires T régulatrices sous ilunocitinib, suggéré par l’absence de perturbation de l’immunophénotype CD4+ dans l’étude de Kuntz (2025), est un argument en faveur de la compatibilité de cette association. Des essais combinés sont en attente pour documenter cette hypothèse.
Les données comparatives avec le lokivetmab et les inhibiteurs de JAK de seconde génération en cours de développement vétérinaire permettront de positionner l’ilunocitinib dans l’algorithme thérapeutique. L’évaluation de biothérapies anti-IL-4Rα canines (analogues au dupilumab humain) constitue un axe de recherche exploratoire. La caractérisation des gènes de susceptibilité à la DAC, en attente de résultats depuis deux décennies, pourrait à terme permettre l’identification de biomarqueurs prédictifs de la réponse thérapeutique aux JAKi. L’étude des pharmacocinétiques de population, intégrant les covariables de race, d’âge, de poids et de fonction hépatique, constitue un complément indispensable aux données actuelles pour optimiser les schémas posologiques individualisés.
L’ilunocitinib s’inscrit dès lors comme une avancée thérapeutique significative dans la prise en charge de la dermatite atopique canine et des dermatites allergiques associées, apportant un profil de tolérance favorable à la dose thérapeutique, une efficacité documentée par des essais contrôlés de haut niveau de preuve, et un schéma posologique simplifié à une prise quotidienne unique. L’accès à des données de pharmacovigilance internationales sur un effectif croissant de chiens traités — plus de 800 000 à la date de septembre 2025, avec un déploiement commercial en Europe, en Amérique du Nord, au Brésil et au Japon — permettra de préciser les manifestations cliniques rares et les interactions médicamenteuses en conditions réelles d’utilisation. L’état des connaissances en 2025-2026 positionne cette molécule comme un outil de première ligne pour le praticien dermatologue et le généraliste confronté aux dermatites allergiques canines, dont l’intégration dans une stratégie thérapeutique multimodale — associant contrôle allergénique environnemental, restauration de la barrière cutanée par des topiques émollients, gestion des surinfections bactériennes et fongiques, et le cas échéant immunothérapie allergénique spécifique — demeure la clé d’une prise en charge optimale et durable de la DAC. Le positionnement du Zenrelia par rapport aux molécules existantes (oclacitinib, lokivetmab, ciclosporine) et aux molécules en développement (atinvicitinib, inhibiteurs sélectifs de seconde génération) se précisera au fil des publications comparatives et des retours d’expérience clinique à large échelle.
Références
Aidasani D, Zaya MJ, Muppal JG, Locuson CW. In vitro drug-drug interaction screening of canine cytochrome P450 enzymes with clomipramine and related tricyclics. Drug Metab Dispos. 2008;36:1512-1518.
Boerngen K, Patel Y, Pittorino M, Toutain CE. Pharmacokinetics of ilunocitinib, a new Janus kinase inhibitor, in dogs. J Vet Pharmacol Ther. 2026;49(1):7–16.
Bonelli M, Kerschbaumer A, Kastrati K, Ghoreschi K, Gadina M, Heinz LX, et al. Selectivity, efficacy and safety of JAKinibs: new evidence for a still evolving story. Ann Rheum Dis. 2024;83:139-160.
Chaudhary SK, Singh SK, Kumari P, Kanwal S, Soman SP, Choudhury S, et al. Alterations in circulating concentrations of IL-17, IL-31 and total IgE in dogs with atopic dermatitis. Vet Dermatol. 2019;30:383-e114.
Choy EH. Clinical significance of Janus kinase inhibitor selectivity. Rheumatology. 2019;58:953-962.
Clark JD, Flanagan ME, Telliez JB. Discovery and development of Janus kinase (JAK) inhibitors for inflammatory diseases. J Med Chem. 2014;57:5023-5038.
Cosgrove SB, Wren JA, Cleaver DM, Walsh KF, Follis SI, King VI, et al. Long-term compassionate use of oclacitinib in dogs with atopic and allergic skin disease: safety, efficacy and quality of life. Vet Dermatol. 2015;26:171-179.
Datsi A, Steinhoff M, Ahmad F, Alam M, Buddenkotte J. Interleukin-31: the “itchy” cytokine in inflammation and therapy. Allergy. 2021;76:2982-2997.
Di Salvo E, Ventura-Spagnolo E, Casciaro M, Navarra M, Gangemi S. IL-33/IL-31 axis: a potential inflammatory pathway. Mediators Inflamm. 2018;2018:3858032.
Drechsler Y, Dong C, Clark DE, Kaur G. Canine atopic dermatitis: prevalence, impact, and management strategies. Vet Med (Auckl). 2024;15:15-29.
EMA. European Public Assessment Report (EPAR) Zenrelia™ (ilunocitinib). European Medicines Agency; 2025.
Favrot C, Fischer N, Olivry T, Zwickl L, Audergon S, Rostaher A. Atopic dermatitis in West Highland White Terriers — Part I: Natural history of atopic dermatitis in the first three years of life. Vet Dermatol. 2020;31:106-110.
FDA. New Animal Drug Application NADA 141-585 Zenrelia™ (ilunocitinib tablets). US Food and Drug Administration; 2024.
Fennis M, Vroom M, Broeckx BJG, Vandenabeele S, De Cock H. Concurrent administration of oclacitinib and allergen-specific immunotherapy in dogs with atopic dermatitis. Vet Dermatol. 2022;33:344-e85.
Fent GM, Despa S, Gabor L, Earll M, McCandless EE, O’Kelley S, et al. Response to primary canine core vaccination in 10-month-old seronegative dogs treated with three times the recommended therapeutic dose of ilunocitinib tablets (Zenrelia™). BMC Vet Res. 2025a;21:461.
Fent GM, Jacela J, Plazola-Ortiz R, Olps J, McCandless EE, Toutain CE, et al. Immunologic response to first booster vaccination in dogs treated with Zenrelia™ (ilunocitinib tablets) at up to three times the recommended therapeutic dose compared to untreated controls. BMC Vet Res. 2025b;21:481.
Forster S, Trout CM, Despa S, Boegel A, Berger D, King S. Efficacy and field safety of ilunocitinib for the control of allergic dermatitis in client-owned dogs: a multicenter, double-masked, randomised, placebo-controlled clinical trial. Vet Dermatol. 2025a;0:1-11.
Forster S, Trout CM, Despa S, Boegel A, Berger D, King S. Efficacy and field safety of ilunocitinib for the control of atopic dermatitis in client-owned dogs: a multicentre, double-masked, randomised, placebo-controlled clinical trial. Vet Dermatol. 2025b;0:1-13.
Forster S, Boegel A, Despa S, Trout C, King S. Comparative efficacy and safety of ilunocitinib and oclacitinib for the control of pruritus and associated skin lesions in dogs with atopic dermatitis. Vet Dermatol. 2025c;36:165-176.
Fukuyama T, Ganchingco JR, Bäumer W. Demonstration of rebound phenomenon following abrupt withdrawal of the JAK1 inhibitor oclacitinib. Eur J Pharmacol. 2017;794:20-26.
Gonzales AJ, Humphrey WR, Messamore JE, Fleck TJ, Fici GJ, Shelly JA, et al. Interleukin-31: its role in canine pruritus and naturally occurring canine atopic dermatitis. Vet Dermatol. 2013;24:48-53.
Gonzales AJ, Bowman JW, Fici GJ, Zhang M, Mann DW, Mitton-Fry M. Oclacitinib (APOQUEL) is a novel Janus kinase inhibitor with activity against cytokines involved in allergy. J Vet Pharmacol Ther. 2014;37:317-324.
Hensel P, Santoro D, Favrot C, Hill P, Griffin C. Canine atopic dermatitis: detailed guidelines for diagnosis and allergen identification. BMC Vet Res. 2015;11:196.
Hillier A, Griffin CE. The ACVD task force on canine atopic dermatitis (I): incidence and prevalence. Vet Immunol Immunopathol. 2001;81:147-151.
Huang JT, Doering KA, Fang X. Mechanism of action underlying the efficacy of JAK inhibitors in skin diseases. J Drugs Dermatol. 2022;21:234-241.
Kuntz EA, Gabor L, Toutain CE. Safety of ilunocitinib tablets (Zenrelia™) after once daily oral administration in dogs. BMC Vet Res. 2025;21:144.
Marsella R. Advances in our understanding of canine atopic dermatitis. Vet Dermatol. 2021;32:547-e151.
Michels GM, Ramsey DS, Walsh KF, Martinon OM, Mahabir SP, Hoevers JD, et al. A blinded, randomized, placebo-controlled, dose determination trial of lokivetmab (ZTS-00103289), a caninized, anti-canine IL-31 monoclonal antibody in client owned dogs with atopic dermatitis. Vet Dermatol. 2016;27:478-e129.
Nemmer JM, Stander S. New developments in the pathophysiology of pruritus. Dermatol Ther (Heidelb). 2021;11:1795-1815.
Olivry T, Bizikova P. A systematic review of the evidence of reduced allergenicity and clinical benefit of food hydrolysates in dogs with cutaneous adverse food reactions. Vet Dermatol. 2010;21:32-41.
Olivry T, Saridomichelakis M, Nuttall T, Bensignor E, Griffin CE, Hill PB, et al. Validation of the canine atopic dermatitis extent and severity index (CADESI)-4, a simplified severity scale for assessing skin lesions of atopic dermatitis in dogs. Vet Dermatol. 2014;25:77-85.
Olivry T, DeBoer DJ, Favrot C, Jackson HA, Mueller RS, Nuttall T, et al. Treatment of canine atopic dermatitis: 2015 updated guidelines from the International Committee on Allergic Diseases of Animals (ICADA). BMC Vet Res. 2015;11:210.
Olivry T, Lokianskiene V, Blanco A, et al. A randomised controlled trial testing the rebound-preventing benefit of four days of prednisolone during the induction of oclacitinib therapy in dogs with atopic dermatitis. Vet Dermatol. 2023;34:99-106.
O’Shea JJ, Schwartz DM, Villarino AV, Gadina M, McInnes IB, Laurence A. The JAK-STAT pathway: impact on human disease and therapeutic intervention. Annu Rev Med. 2015;66:311-328.
Payne JT, Danielson JR, Bennett BS, Wheeler J, Krebber R. Interaction of transporter proteins with P-glycoprotein inhibitors and substrates in vitro. Drug Metab Dispos. 2015;43:1199-1207.
Pucheu-Haston CM, Bizikova P, Marsella R, Santoro D, Nuttall T, Eisenschenk MN. Review: Genetics, epigenetics and allergy of canine atopic dermatitis. Vet Dermatol. 2015;26:84-e26.
Santoro D, Marsella R, Pucheu-Haston CM, Eisenschenk MN, Nuttall T, Bizikova P. Review: Pathogenesis of canine atopic dermatitis: skin barrier and host-micro-organism interaction. Vet Dermatol. 2015;26:84-e25.
Spinelli FR, Meylan F, O’Shea JJ, et al. JAK inhibitors: ten years after. Eur J Immunol. 2021;51:1615-1627.
Steffan J, Favrot C, Mueller R. A systematic review and meta-analysis of the efficacy and safety of cyclosporin for the treatment of atopic dermatitis in dogs. Vet Dermatol. 2006;17:3-16.
Strober B, Buonanno M, Clark JD, et al. Effect of tofacitinib, a Janus kinase inhibitor, on haematological parameters during 12 weeks of psoriasis treatment. Br J Dermatol. 2013;169:992-999.
Virtanen A, Palmroth M, Liukkonen S, et al. Differences in JAK isoform selectivity among different types of JAK inhibitors evaluated for rheumatic diseases through in vitro profiling. Arthritis Rheumatol. 2023;75:2054-2061.